题目内容
某化学反应2X(g)?Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol.L-1)随反应时间(min)的变化情况如下表:
下列说法不正确的是( )
| 实验 序号 |
时间 浓度 温度 |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A、前10分钟,实验4的平均化学反应速率比实验1的大 |
| B、实验2可能使用了催化剂 |
| C、C>1.0 |
| D、实验3比实验2先达到化学平衡状态 |
分析:A、实验4和实验1在10分钟都未达到平衡,依据化学反应速率概念计算进行比较判断;
B、实验2和实验1达到相同的平衡状态,但实验2所需时间短说明可能使用了催化剂;
C、实验3达到平衡X的浓度大于实验1,温度相同说明X起始浓度大于1.0mol/L;
D、依据图表数据分析,实验3在40min时X浓度不变达到平衡,实验2在20min时达到平衡.
B、实验2和实验1达到相同的平衡状态,但实验2所需时间短说明可能使用了催化剂;
C、实验3达到平衡X的浓度大于实验1,温度相同说明X起始浓度大于1.0mol/L;
D、依据图表数据分析,实验3在40min时X浓度不变达到平衡,实验2在20min时达到平衡.
解答:解:A、实验4和实验1在10分钟都未达到平衡,依据化学反应速率概念计算,实验1X的反应速率=
=0.02mol/L?min,实验4X的反应速率=
=0.06mol/L?min,所以实验4反应速率大于实验1,故A正确;
B、实验2和实验1达到相同的平衡状态,但实验2所需时间短说明可能使用了催化剂,催化剂改变反应速率不改变化学平衡,故B正确;
C、实验3达到平衡X的浓度大于实验1,温度相同,达到平衡说明X起始浓度大于1.0mol/L,故C正确;
D、依据图表数据分析,实验3在40min时X浓度不变达到平衡,实验2在20min时达到平衡,实验2达到平衡快,故D错误;
故选D.
| 1.0mol/L-0.8mol/L |
| 10min |
| 1.0mol/L-0.4mol/L |
| 10min |
B、实验2和实验1达到相同的平衡状态,但实验2所需时间短说明可能使用了催化剂,催化剂改变反应速率不改变化学平衡,故B正确;
C、实验3达到平衡X的浓度大于实验1,温度相同,达到平衡说明X起始浓度大于1.0mol/L,故C正确;
D、依据图表数据分析,实验3在40min时X浓度不变达到平衡,实验2在20min时达到平衡,实验2达到平衡快,故D错误;
故选D.
点评:本题考查了化学平衡影响因素分析判断,主要是数据分析判断,平衡标志的理解应用,题目难度中等.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
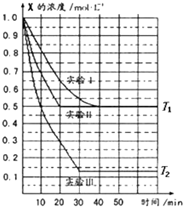
 (2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( )
(2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( )