题目内容
1molO2与1molCO2相比较,下列叙述中正确的是( )A.在同温同压下,体积相等
B.在同温同压下,密度相等
C.在标准状况下,质量相等
D.所含原子数相等
【答案】分析:相同条件下,气体的Vm相等,根据n=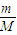 =
=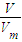 结合分子的组成判断.
结合分子的组成判断.
解答:解:A.在同温同压下,气体的Vm相等,由V=n×Vm可知,体积相等,故A正确;
B.由n=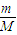 =
=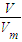 可知:ρ=
可知:ρ=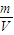 =
=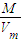 ,则密度与气体的相对分子质量呈正比,二者的相对分子质量不同,则密度不同,故B错误;
,则密度与气体的相对分子质量呈正比,二者的相对分子质量不同,则密度不同,故B错误;
C.由n=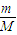 ,二者的摩尔质量不等,则质量不等,故C错误;
,二者的摩尔质量不等,则质量不等,故C错误;
D.由N=nNA知,相同物质的量时,气体的分子数相等,但原子数不等,故D错误.
故选A.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意相关物质的量的计算公式的运用.
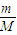 =
=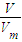 结合分子的组成判断.
结合分子的组成判断.解答:解:A.在同温同压下,气体的Vm相等,由V=n×Vm可知,体积相等,故A正确;
B.由n=
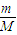 =
=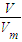 可知:ρ=
可知:ρ=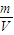 =
=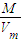 ,则密度与气体的相对分子质量呈正比,二者的相对分子质量不同,则密度不同,故B错误;
,则密度与气体的相对分子质量呈正比,二者的相对分子质量不同,则密度不同,故B错误;C.由n=
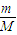 ,二者的摩尔质量不等,则质量不等,故C错误;
,二者的摩尔质量不等,则质量不等,故C错误;D.由N=nNA知,相同物质的量时,气体的分子数相等,但原子数不等,故D错误.
故选A.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意相关物质的量的计算公式的运用.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
下列叙述中,正确的是( )
| A、20℃时,1molSO2的体积一定大于22.4L | B、1mol/LNaCl溶液表示1L水中含有NaCl58.5g | C、常温下,1molCO2与1molH2O所含有的分子总数和原子总数均相等 | D、1molO2与足量金属钠反应,得到了4mole- |