题目内容
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列说法正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列说法正确的是( )分析:A.由图可知,10s内Z的物质的量变化量为1.58mol,根据v=
计算v(Z);
B.根据图象中变化求X的物质的量浓度变化;
C.根据转化率=
×100%计算;
D.根据物质的量的变化,判断出反应物、生成物及是否是可逆反应,利用物质的量之比化学计量数之比书写方程式.
| △n | ||
|
B.根据图象中变化求X的物质的量浓度变化;
C.根据转化率=
| 转化量 |
| 起始量 |
D.根据物质的量的变化,判断出反应物、生成物及是否是可逆反应,利用物质的量之比化学计量数之比书写方程式.
解答:解:A.10s内,用Z表示的反应速率为v(Z)=
=0.079moL/(L?s),故A错误;
B.由图象可知X反应了1.20mol-0.41mol=0.79mol,所以X的物质的量浓度减少了
=0.395mol/L,故B错误;
C、反应开始到10s,反应的Y的物质的量为0.79mol,则Y的转化率为
=79.0%,故C错误;
D、在反应中,X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,则X、Y为反应物,Z为生成物,相同时间内物质的量的变化比值为
c(X):c(Y):c(Z)=(1.20-0.41):(1.00-0.21):1.58=1:1:2,化学反应中物质的量变化之比等于化学剂量数之比,
则化学方程式为X(g)+Y(g) 2Z(g),故D正确;
2Z(g),故D正确;
故选D.
| 1.58mol | ||
|
B.由图象可知X反应了1.20mol-0.41mol=0.79mol,所以X的物质的量浓度减少了
| 0.79mol |
| 2L |
C、反应开始到10s,反应的Y的物质的量为0.79mol,则Y的转化率为
| 0.79mol |
| 1.00mol |
D、在反应中,X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,则X、Y为反应物,Z为生成物,相同时间内物质的量的变化比值为
c(X):c(Y):c(Z)=(1.20-0.41):(1.00-0.21):1.58=1:1:2,化学反应中物质的量变化之比等于化学剂量数之比,
则化学方程式为X(g)+Y(g)
 2Z(g),故D正确;
2Z(g),故D正确;故选D.
点评:本题考查化学平衡的变化图象,题目难度不大,本题注意化学方程式的确定方法,平衡状态的判断以及反应速率和转化率的计算,把握好相关概念和公式的理解及运用.

练习册系列答案
相关题目
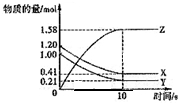 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )| A、反应开始到10s,用Z表示的反应速率为0.158moL/(L?s) | B、l0s后,该反应停止进行 | C、反应的化学方程式为:X(g)+Y(g)?2Z(g) | D、反应开始到l0s时,平均反应速率ν(X)=ν(Y)=0.0395mol/(L?s) |
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 2Z(g)
2Z(g)
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.回答下列问题:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.回答下列问题: 2Z
2Z