题目内容
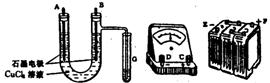
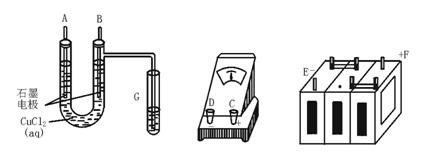
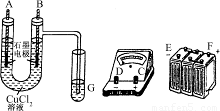
某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数值,其实验方案的要点为:①用直流电电解氯化铜溶液,所用仪器如图所示。

②在电流强度为IA,通过时间为ts后,精确测得某电极上析出的铜的质量为mg。
试回答:(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示。下同) E接________,C接________,________接F。
线路中的电流方向为_______→_______→_______→_______→C→_______→_______。
(2)写出B电极上发生反应的离子方程式________G试管中淀粉KI溶液变化的现象为________,相应的离子方程式是________。
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序应是________。(选填下列操作步骤的编号)
①称量电解前电极重量,②刮下电解后电极上的铜并清洗,③用蒸馏水清洗电解后电极,①低温烘干电极后称量,⑤低温烘干刮下的铜后称量,⑥再次低温烘干后称量至恒重。
(4)已知电子的电量为1.6×10-19C。试列出阿伏伽德罗常数的计算表达式![]() =_______。
=_______。
答案:
解析:
提示:
解析:
| (1)E接D,C接A,B接F。F→B→A→C→D→E。
(2)2Cl-+2e=Cl2↑,溶液变蓝色Cl2+2I-=I2+2Cl-。 (3)①③④⑥ (4)
|
提示:
| 解答此题,要运用物理知识与技能完成仪器的连接(A接电源负极,B接电源正极);判断线路中电流方向(从电源正极沿电路流向负极);根据化学反应原理(B极发生氧化反应)书写有关的离子反应式;依据阴极析出Cu的质量(m)与电极上通过电量(I·t)关系:
|

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目