题目内容
(10分)
高炉炼铁过程中发生的主要反应为:
1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
|
温度/℃ |
1000 |
1150 |
1300 |
|
平衡常数 |
4.0 |
3.7 |
3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0min后达到平衡,则该时间范围内反应的平均反应速率υ(CO2)= ,CO的平衡转化率= ;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 。
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
(1)K平=[c(CO2)]/[c(CO)] (2分)< (2分)
(2)0.006mol/(L·min) (2分) 60%或0.6 (2分) (3)C (2分)
【解析】考查平衡常数的判断及有关应用。
(1)平衡常数是在一定条件下,当可逆反应达到化学平衡时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以该反应的平衡常数表达式为K平=[c(CO2)]/[c(CO)]。随着温度的升高,平衡常数逐渐减小,所以正反应是放热反应,即△H小于0。
(2)
1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
起始量(mol) 1.0 1.0
转化量(mol) x x
平衡量(mol) 1.0-x x+10
所以有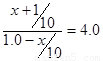 ,解得x=0.6mol
,解得x=0.6mol
所以该时间范围内反应的平均反应速率υ(CO2)=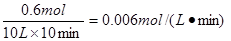
CO的平衡转化率=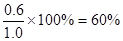
(3)由于反应前后体积不变,铁和氧化铁是固体,所以选项ABEF对平衡不影响。正反应放热,升高温度,平衡向逆反应方向移动,转化率降低,所以正确的答案是C。

高炉炼铁过程中发生的反应:
|
| 1 |
| 3 |
| 2 |
| 3 |
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
| A、△H<0 | ||
B、该反应的平衡常数表达式是K=
| ||
| C、其他条件不变,向平衡体系充入CO2气体,K值减小 | ||
| D、其他条件不变,升高温度,可以降低CO的平衡转化率 |