题目内容
下列元素的氧化物的水化物碱性最强的是
- A.Ca
- B.Na
- C.Ba
- D.Cs
解析:碱性最强的一定是元素的金属性最强的.Na与Cs同处一族,金属性Cs>Na;Ca与Ba同处一族,Ba>Ca;Cs与Ba同处同一周期,Cs>Ba.故CsOH的碱性最强.

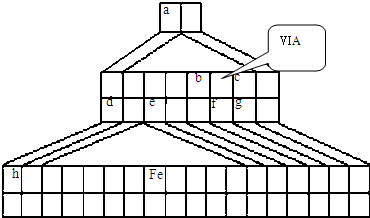
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5。则两种水溶液中由水电离出的H+浓度之比是 。
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解。写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式 。
(3)A、B、D、E四种元素组成的某无机化合物浓度为 0.1 mol/L时, pH最接近 。
A.5.6 B.7.0 C.8.4 D.13.0
(4)化学反应3A2(g)+C2(g)![]() 2CA3(g)。ΔH=-92.4kJ·mol-1
2CA3(g)。ΔH=-92.4kJ·mol-1
|
和CA3的量),右图表示反应速率与反应过程的关
系,其中表示平衡混合物中CA3的含量最高的一段
时间是 。
②温度为T℃时,将4amolA2和2a molC2放入1L
密闭容器中,充分反应后测得C2的转化率为50%,
则反应的平衡常数 。
③在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molC2和3molA2,充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是________ ____;
(5)已知0.4mol 液态C2 A4与足量的液态双氧水反应,生成C2和水蒸气,放出256.65 kJ
的热量。写出该反应的热化学方程式 。

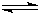 NH3?H2O+H+
NH3?H2O+H+

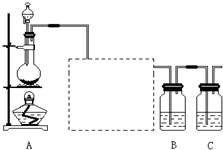 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
