题目内容
一定量的铁与稀盐酸反应,生成了4.48L(STP)氢气。
(1)计算发生反应的氯化氢和铁的物质的量分别为多少?
(2)若所用盐酸的浓度为0.5 mol·L-1,则至少需要盐酸的体积为多少升?
(1)计算发生反应的氯化氢和铁的物质的量分别为多少?
(2)若所用盐酸的浓度为0.5 mol·L-1,则至少需要盐酸的体积为多少升?
(6分)
解:n(H2) =4.48L/22.4L· mol-=0.2 mol (1分)
(1分)
Fe+2HCl ="=" Fe Cl2+H2 ↑ (1分)
Fe Cl2+H2 ↑ (1分)
 1 2 1
1 2 1
n(Fe) n(HCl) 0.2 mol
列比例式,计算得:
n(Fe) =0.2 mol (1分)
n(HCl) =0.4 mol(1分)
v(HCl) =0.4 mol/0.5 mol/L=0 .8L(2分)
.8L(2分)
解:n(H2) =4.48L/22.4L· mol-=0.2 mol
 (1分)
(1分)Fe+2HCl ="="
 Fe Cl2+H2 ↑ (1分)
Fe Cl2+H2 ↑ (1分) 1 2 1
1 2 1n(Fe) n(HCl) 0.2 mol
列比例式,计算得:
n(Fe) =0.2 mol (1分)
n(HCl) =0.4 mol(1分)
v(HCl) =0.4 mol/0.5 mol/L=0
 .8L(2分)
.8L(2分)略

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
 mol/L
mol/L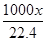 mol/L
mol/L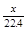 mol/L
mol/L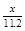 mol/L
mol/L