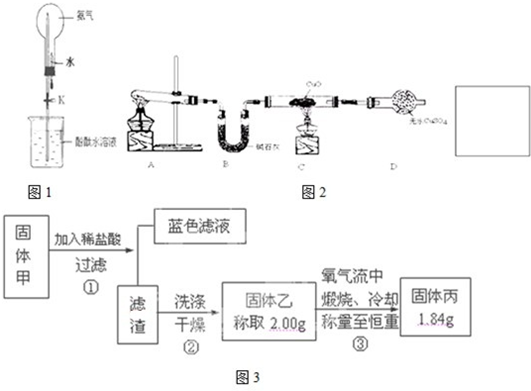
题目内容
amol Cu与含bmol HNO3的硝酸溶液恰好完全反应,则被还原的HNO3物质的量一定是( )A.(b-2a)mol B.![]() mol C.
mol C.![]() mol D.2amol
mol D.2amol
答案:A
解析:
解析:
| 错选:B或C
错因:根据常规思维,3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O Cu+4HNO3(浓) ====Cu(NO3)2+2NO2↑+2H2O用极限法解题,全被还原为NO时,被还原HNO3为b∕2mol,全被还原为NO2,被还原HNO3为b∕4mol,从而选C或B.题目是求被还原HNO3一定为多少,这里C在
|

练习册系列答案
相关题目
现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为amol,Cu的物质的量分数为x;研成粉末后,全部投入含bmol HNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:(已知:Cu+2Fe3+=2Fe2++Cu2+)
(1)随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有六种情况,请用粒子符号填写下列空白:
| ① | ② | ③ | ④ | ⑤ | ⑥ |
溶液中的金属离子 |
| Fe2+ |
| Fe2+、Cu2+ |
| Cu2+、Fe3+ |
残留固体成分 | Fe、Cu |
| Cu | ―― | ―― | ―― |
(2)当溶液中金属离子只有Fe2+、Cu2+时,求b的取值范围。
(3)当x=0.5时,溶液中Fe3+与Fe2+的物质的量相等时,在标准状况共产生672mL气体。求a、b的值。