��Ŀ����
��һ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��N2��0.6 mol��H2����һ�������·�����Ӧ��N2(g)��3H2(g) 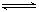 2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
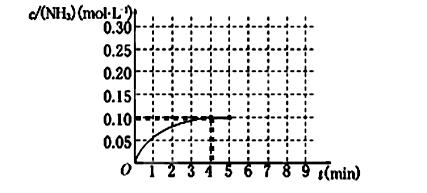
��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��������ƽ����Ӧ����v(H2)Ϊ______________��
��2���÷�Ӧ�ﵽƽ��ʱN2��ת����_________________��
��3����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ____________��(�����)
a��0.20 mol��L��1 b��0.12 mol��L��1 c��0.10 mol��L��1 d��0.08 mol��L��1
��4����д���÷�Ӧ��ƽ�ⳣ������ʽ_________�����÷�Ӧ��298K��398Kʱ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������="��" �� ������ ����
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ��(��ʱNH3��Ũ��ԼΪ0.25 mol��L��1)��������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߡ�
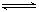 2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��������ƽ����Ӧ����v(H2)Ϊ______________��
��2���÷�Ӧ�ﵽƽ��ʱN2��ת����_________________��
��3����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ____________��(�����)
a��0.20 mol��L��1 b��0.12 mol��L��1 c��0.10 mol��L��1 d��0.08 mol��L��1
��4����д���÷�Ӧ��ƽ�ⳣ������ʽ_________�����÷�Ӧ��298K��398Kʱ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������="��" �� ������ ����
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ��(��ʱNH3��Ũ��ԼΪ0.25 mol��L��1)��������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߡ�
��1��0.0375 mol��L��1��min��1
��2��50%
��3��a��c
��4��
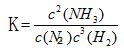 >
>��5��
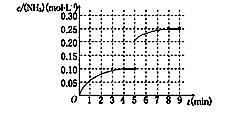
�����������1��v(H2)="3/2" v(NH3)=3/2��0.10mol/L��4min=0.0375 mol��L��1��min��1��
N2(g)��3H2(g)
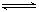 2NH3(g)
2NH3(g)��ʼŨ�ȣ�mol?L?1��0.1 0.3 0
��ʼŨ�ȣ�mol?L?1��0.05 0.15 0.1
��ʼŨ�ȣ�mol?L?1��0.05 0.15 0.1
��÷�Ӧ�ﵽƽ��ʱN2��ת����=0.05mol?L?1��0.1mol?L?1��100%=50%
��3�����ݻ�ѧ����ʽ��֪NH3��Ũ�ȷ�Χ0<c(NH3)<0.2mol?L?1��ԭƽ��NH3��Ũ��Ϊ0.10mol?L?1���¶ȸı䣬ƽ���ƶ��ᷢ���ƶ�����ƽ���Ũ��һ������0.10mol?L?1����a��c����ܡ�
��4������ƽ�ⳣ���Ķ���ɵø÷�Ӧ��ƽ�ⳣ������ʽΪ��
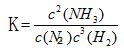 ����Ϊ����ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С������K1>K2��
����Ϊ����ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С������K1>K2����5����5����ĩ�������������Сһ���NH3��Ũ�ȱ�Ϊ0.20mol?L?1��ѹǿ����ƽ�������ƶ���NH3��Ũ�������ӣ���8minĩΪ0.25mol?L?1�����ɻ������ߡ�

��ϰ��ϵ�д�
 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
�����Ŀ
 H2+I2
H2+I2
 2SO3(g) + Q�����˷�Ӧ��ʼ�����ʵ�����ͬ�������й�ϵͼ��ȷ����_________ (�����)
2SO3(g) + Q�����˷�Ӧ��ʼ�����ʵ�����ͬ�������й�ϵͼ��ȷ����_________ (�����)
 2C(g) ��H��0�������Ӧ����ȷͼ��Ϊ�� ��
2C(g) ��H��0�������Ӧ����ȷͼ��Ϊ�� ��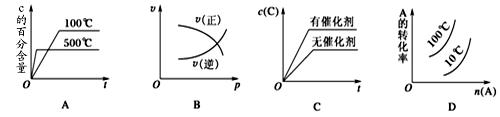
 A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
 2XY��g�� ��H<0���ﵽ��ƽ�⡣�ڽ��ı�ijһ�����ﵽ��ƽ�⣬�Դ˹��̵ķ�����ȷ����( )
2XY��g�� ��H<0���ﵽ��ƽ�⡣�ڽ��ı�ijһ�����ﵽ��ƽ�⣬�Դ˹��̵ķ�����ȷ����( )
 2NH3(g)��Q��Q��0��,
2NH3(g)��Q��Q��0��, 



 2Z(g)��H��0���÷�Ӧ�����ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ����ͼ��ʾ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵij�ʼ��������������˵���д������
2Z(g)��H��0���÷�Ӧ�����ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ����ͼ��ʾ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵij�ʼ��������������˵���д������
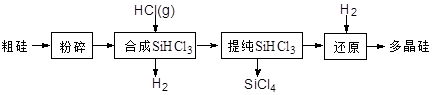
 Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��
Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� �� H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
 2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ ��
2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ ��