题目内容
12.甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为CO(g)+2H2(g)?CH3OH(g)△H.(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间的变化如图甲所示.

①从反应开始到5min,用氢气表示的平均反应速率v(H2)=0.6mol/(L•min).
②下列说法正确的是AB(填序号).
A.达到平衡时,H2的转化率为75%
B.5min后容器中压强不再改变
C.达到平衡后,再充入氩气,反应速率增大
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH2,达到平衡时容器体积为2L,且含有0.4molCH3OH(g),则该反应平衡常数的值为50,此时向容器中再通入0.35molCO气体,则此平衡将逆向移动(填“正向移动”“不移动”或“逆向移动”)
(3)若压强、投料比$\frac{x}{n({H}_{2})}$对反应的影响如图乙所示,则图中曲线所示的压强关系:p1<p2(填“=”“>”或“<”),其判断理由是正反应体积减小,投料比相同时,增大压强平衡正向移动,氢气的量减小.
(4)甲醇是一种新型的汽车动力燃料.已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ•mol-1.
(5)现有容积均为1L的a、b、c三个密闭容器,往其中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图丙所示.b中甲醇体积分数大于a中的原因是b中温度高,反应速率快,反应相同时间生成的甲醇多,体积分数大.达到平衡时,a、b、c中CO的转化率大小关系为a>b>c.
(6)甲醇作为一种燃料还可用于燃料电池.在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质.该电池的负极反应式为CH3OH-6e-+3CO32-=4CO2↑+2H2O.
分析 (1)①图象中计算一氧化碳和甲醇浓度变化,结合化学方程式定量关系计算氢气变化浓度,反应速率c=$\frac{△c}{△t}$;
②A.结合化学三行计算列式计算分析判断;
B.5min后浓度不变说明反应达到平衡状态;
C.恒温恒容条件下反应达到平衡后,再充入氩气,总压增大分压不变,速率不变;
D.5min前反应正向进行;
(2)根据平衡常数的计算公式计算,恒温恒压下,体积之比等于物质的量之比,据此计算加入0.35molCO时容器的体积,计算此时浓度商,与平衡常数相比判断反应进行方向;
(3)正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,氢气的含量降低;
(4)根据CO和CH3OH的燃烧热先书写热方程式,再利用盖斯定律来分析甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式;
(5)未到达平衡前,升高温度甲醇的含量增大,到达平衡后再升高温度,平衡向逆反应方向移动,甲醇的含量降低,而5min时,b容器中甲醇的含量不一定最高,不一定是平衡状态,达到平衡时,a、b、c三个容器的反应温度不同,a容器温度最低,c容器的反应温度最高,根据反应放热可判断出;
(6)负极上CH3OH失电子结合碳酸根发生氧化反应生成二氧化碳和水.
解答 解:(1)①从反应开始到5min,图象中一氧化碳浓度变化=2.0mol/L-0.5mol/L=1.5mol/L,CO(g)+2H2(g)?CH3OH(g),氢气浓度变化3mol/L,
用氢气表示的平均反应速率v(H2)=$\frac{3mol/L}{5min}$=0.6mol/(L•min),
故答案为:0.6mol/(L•min);
②A.达到平衡时,H2的转化率=$\frac{3mol/L}{4mol/L}$×100%=75%,故A正确;
B.5min后浓度不变说明反应达到平衡状态,5min后容器中压强不再改变,故B正确;
C.恒温恒容条件下反应达到平衡后,再充入氩气,总压增大分压不变,速率不变,故C错误;
D.5min前反应正向进行,2min前后v(正)>v(逆),故D错误;
故答案为:AB;
(2)CO(g)+2H2(g)?CH3OH(g)
起始:1.2mol 1mol 0
转化:0.4mol 0.8mol 0.4mol
平衡:0.8mol 0.2mol 0.4mol
所以:k=$\frac{0.2}{0.4×0.{1}^{2}}$=50(mol/L)-2,
此时向容器中再通入0.35molCO气体,假设平衡不移动时,此时容器体积为:2L×$\frac{(0.35+0.8+0.2+0.4)mol}{(0.8+0.2+0.4)mol}$=2.5L,则浓度商Qc=$\frac{\frac{0.4}{2.5}}{\frac{1.15}{2.5}×(\frac{0.2}{2.5})^{2}}$=54.3,大于平衡常数50,平衡向逆反应方向移动,
故答案为:50;逆反应方向;
(3)由图可知,压强P1时的百分含量大于压强P2的百分含量,由于正反应为气体体积减小的反应,正反应体积减小,投料比相同时,增大压强平衡正向移动,氢气的量减小,故压强P1<P2,
故答案为:<;正反应体积减小,投料比相同时,增大压强平衡正向移动,氢气的量减小;
(4)由CO(g)和CH3OH(l)的燃烧热△H分别为-283.0kJ•mol-1和-726.5kJ•mol-1,则
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1
由盖斯定律可知,②-①得反应CH3OH(l)+O2(g)=CO(g)+2 H2O(l),则△H=-726.5kJ•mol-1-(-283.0kJ•mol-1)=-443.5kJ•mol-1,
故答案为:CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-443.5kJ•mol-1;
(5)未到达平衡前,升高温度甲醇的含量增大,到达平衡后再升高温度,平衡向逆反应方向移动,甲醇的含量降低,b中甲醇体积分数大于a中的原因:b中温度高,反应速率快,反应相同时间生成的甲醇多,体积分数大,达到平衡时,a、b、c三个容器的反应温度不同,a容器温度最低,c容器的反应温度最高,根据反应放热可判断出,升高温度,平衡逆向移动,甲醇的体积分数减小,故应为a>b>c,
故答案为:b中温度高,反应速率快,反应相同时间生成的甲醇多,体积分数大 a>b>c;
(6)负极上CH3OH失电子结合碳酸根发生氧化反应生成二氧化碳和水,电极反应式为:CH3OH-6e-+3CO32-=4CO2↑+2H2O,
故答案为:CH3OH-6e-+3CO32-=4CO2↑+2H2O.
点评 本题考查化学平衡常数、反应速率计算、含义及影响因素、热化学方程式的书写、反应进行方向的判断、电极反应式书写等,侧重考查学生对知识的迁移应用,难度中等.

| A. | 塑料 | B. | 蛋白质 | C. | 淀粉 | D. | 葡萄糖 |
| A. | 乙烯的结构简式:CH2CH2 | B. | 苯的最简式:(CH)6 | ||
| C. | 甲烷的空间构型: | D. | 甲基(-CH3)的电子式: |
| A. | 瓶中气体的黄绿色逐渐变浅 | |
| B. | 瓶内壁有油状液滴形成 | |
| C. | 此反应的生成物只有一氯甲烷 | |
| D. | 此反应的液态生成物为二氯甲烷、三氯甲烷及四氯化碳的混合物 |
(1)请写出羟基自由基的电子式

(2)羟基自由基的氧化能力仅次于氟,可以与大多数有机污染物发生快速的链式反应,无选择性地把有害物质氧化成CO2、H2O,请写出羟基自由基与废水中苯酚反应的方程式C6H6O+28•OH═6CO2↑+17H2O.
(3)已知Fe3++SCN=Fe (SCN)2+,在一定温度下该反应达到平衡时c (Fe3+)=0.04mol/L,c (SCN-)=0.1mol/L,c[Fe (SCN) 2+]=0.68mol/L,则此温度下该反应的平衡常数K=170L/mol.有同学利用该反应来检验Fenton试剂中是否产生Fe3+,你认为该办法是否可行,请说明理由不可行,羟基自由基会氧化SCN-.
(4)现运用Fenton试剂降解有机污染物p-CP,试探究有关因素对该降解反应速率的影响.实验中控制p-CP的初始浓度相同,恒定实验温度在298K或313K (其余实验条件 见下表)设计如下对比实验.
| 实验编号 | 实验目的 | T/K | pH | c/10-3mol•L-1 | |
| H2O2 | Fe2+ | ||||
| I | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| II | 探究温度对降解速率的影响 | ① | ② | ③ | ④ |
| III | ⑤ | 298 | 10 | 6.0 | 0.30 |
(5)实验测得p-CP的浓度随时间变化的关系如图所示.
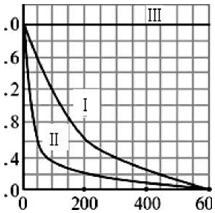
a请根据上图实验I曲线,计算降解反应在50-300s内的平均反应速率v (p-CP)=4.8×10-6mol/(L•s),以及300s时p-CP的降解率为80%;
b.实验I、II表明温度升高,降解反应速率增大(填“增大”、“减小”或“不变”);
c.实验III得出的结论是:pH=10时,反应基本停止.
 0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.
0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.①在图中a表示向稀醋酸中不断加水,b表示向稀醋酸中慢慢滴加0.10mol•Lˉ1的稀氢氧化钠溶液.a中醋酸电离百分率的变化图线已画出,请你图中画出b过程中醋酸电离百分率的变化图线.
②一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| 醋酸浓度(mol•L-1) | 1 | 0.1 | 0.01 |
| pH值 | 2.50 | 3.00 | 3.50 |
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 原子半径:T>Q>R | |
| B. | Q元素在自然界中没有游离态 | |
| C. | 最高价氧化物对应水化物的酸性:Q<W | |
| D. | 气态氢化物的热稳定性:Q>R |
 ,与CO互为等电子体且带1个单位负电荷的阴离子化学式为CN-.
,与CO互为等电子体且带1个单位负电荷的阴离子化学式为CN-.
