题目内容
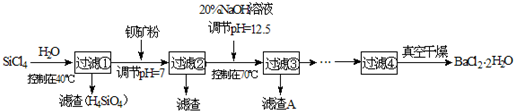
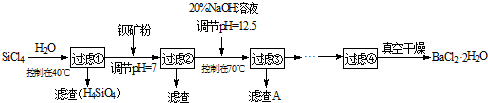
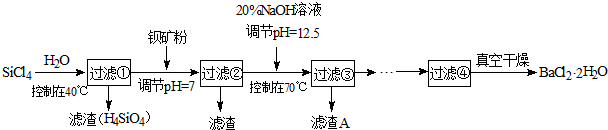
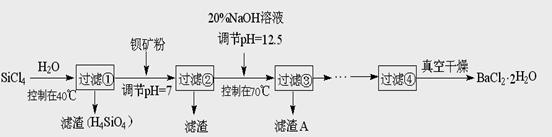
多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它对环境污染很大,能遇水强烈水解,放出大量的热.研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,且含有铁、镁等离子)制备BaCl2·2H2O,工艺流程如下.已知:①常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4.
②M(BaCO3)=197 g/mol,M(BaCl2·2H2O)=244 g/mol

(1)SiCl4水解反应的方程式为________.
已知:SiCl4(s)+H2(g) SiHCl3(s)+HCl(g) ΔH1=+47 kJ/mol
SiHCl3(s)+HCl(g) ΔH1=+47 kJ/mol
SiHCl3(s)+H2(g) Si(s)+3HCl(g) ΔH2=+189 kJ/mol
Si(s)+3HCl(g) ΔH2=+189 kJ/mol
则由SiCl4制备硅的热化学方程式为________.
(2)加钡矿粉并调节pH=7的作用是使BaCO3转化为BaCl2和________.
(3)加20% NaOH调节pH=12.5,得到滤渣A的主要成分是________.
(4)BaCl2滤液经________、________、过滤、洗涤,再经真空干燥后得到BaCl2·2H2O.
(5)10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2·2H2O________吨.
答案:
解析:
解析:
|
(1)SiCl4+4H2O (2)使Fe3+完全沉淀(3分) (3)Mg(OH)2(2分) (4)蒸发浓缩、降温结晶(2分) (5)9.76(3分) |

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
 H4SiO4↓+4HCl(本空符号不作扣分要求)(3分) SiCl4(s)+2H2(g)
H4SiO4↓+4HCl(本空符号不作扣分要求)(3分) SiCl4(s)+2H2(g) Si(s)+4HCl(g) ΔH=+236 kJ/mol(3分)
Si(s)+4HCl(g) ΔH=+236 kJ/mol(3分)