题目内容
下列实验选用的用品一定不需要的是
- A.碳酸钠溶液pH值测定(pH试纸)
- B.粗盐提纯(蒸发皿)
- C.蒸馏自来水制蒸馏水(冷凝管)
- D.硝酸钾与食盐的分离(分液漏斗)
分析:A.可用pH试纸测定溶液的pH;
B.粗盐的提纯用到蒸发操作;
C.蒸馏操作用到冷凝管;
D.硝酸钾与食盐的分离用重结晶的方法分离.
解答:A.碳酸钠溶液pH值测定可用pH试纸或pH计,故A不选;
B.粗盐的提纯用到蒸发操作,应用到蒸发皿,故B不选;
C.蒸馏操作用到冷凝管,故C不选;
D.硝酸钾与食盐的分离用重结晶的方法分离,可用过滤的方法分离,不用分液漏斗,故D选.
故选D.
点评:本题考查较为综合,涉及pH的测定,物质的分离和提纯等基本实验操作,题目难度不大,注意常见基本操作的原理、方法和仪器的使用等问题的积累.

实验用品:
仪器:电子天平、砂纸、水槽、100 mL烧杯、铁架台、单孔橡皮塞(玻璃管上带橡胶管和止水夹)、铜丝、30 mL酸式滴定管、100 mL小口径测气管(见下图)。
![]()
药品:镁条、水、15 mol·L-1的浓硫酸。
(1)本实验用0.6 mol·L-1的硫酸进行反应,活动小组共需要480 mL该浓度的硫酸,写出用15 mol·L-1的浓硫酸配制0.6 mol·L-1的硫酸时,还用到的仪器名称和规格____________、____________、____________;需要15 mol·L-1的浓硫酸____________mL。
(2)选用上述仪器的药品进行实验,补写下列实验步骤:
①取一段镁条,擦去氧化膜,称量;
②用细铜丝包裹镁条,铜丝的另一端插在单孔橡皮塞(玻璃管上带橡胶管和止水夹)上;
③_____________________________________________________________;
④_____________________________________________________________;
⑤_____________________________________________________________;
⑥待镁条全部反应后,放置一段时间,调节测气管中水面高度,使管中水面与水槽中水面相平,读出氢气体积。
(3)问题讨论:
①在标准状况下,其他操作都正常,为了保证实验成功,取用的镁条质量应小于_________________g,所用的稀硫酸应大于_________________mL。
②在标准状况下,某学生进行了5次实验,将实验数据通过计算,结果如下:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
H2的体积(L·mol-1) | 23.45 | 22.41 | 22.38 | 22.39 | 22.42 |
则通过实验验证,标准状况下,1 mol H2的体积为____________L。
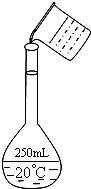 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯 ②100mL量筒 ③500mL容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码)
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯 ②100mL量筒 ③500mL容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码) 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有: 某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.
某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.