题目内容
在恒温恒容下发生反应:N2(g)+3H2(g)
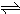
2NH3(g)△H<0.下列判断不正确的是( )
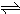
2NH3(g)△H<0.下列判断不正确的是( )
| A.30s内,H2的浓度改变了0.30mol/L,则平均反应速率υ(N2)=0.01mol/(L?s) |
| B.当气体总压不随时间改变时,表明该反应达到平衡状态 |
| C.使用铁触媒可明显减少达到平衡的时间 |
| D.降温可提高N2的转化率 |
A、30s内,H2的浓度改变了0.30mol/L,根据化学反应速率之比等于化学计量数之比,
则平均反应速率υ(N2)=
v(H2)=
×
=
×
=0.0033mol/(L?s),故A错误;
B、当反应达到平衡时,正逆反应反应速率相等,各物质的浓度、物质的量不再发生改变,因反应前后气体的化学计量数之和不相等,则平衡时压强不再改变,故B正确;
C、加入催化剂可加快反应速率,故C正确;
D、该反应的正反应为放热反应,降低温度,平衡向正反应方向移动,故D正确.
故选A.
则平均反应速率υ(N2)=
| 1 |
| 3 |
| 1 |
| 3 |
| △c |
| △t |
| 1 |
| 3 |
| 0.3mol/L |
| 30s |
B、当反应达到平衡时,正逆反应反应速率相等,各物质的浓度、物质的量不再发生改变,因反应前后气体的化学计量数之和不相等,则平衡时压强不再改变,故B正确;
C、加入催化剂可加快反应速率,故C正确;
D、该反应的正反应为放热反应,降低温度,平衡向正反应方向移动,故D正确.
故选A.

练习册系列答案
相关题目
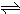 2NH3(g)△H<0.下列判断不正确的是( )
2NH3(g)△H<0.下列判断不正确的是( ) 2NH3(g)△H<0.下列判断不正确的是( )
2NH3(g)△H<0.下列判断不正确的是( )