题目内容
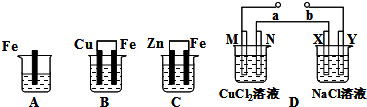
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。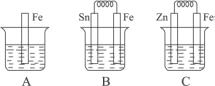
(1)A中反应的离子方程式为__________________________________________________。
(2)B中Sn极的电极反应为___________,Sn极附近溶液的pH(填“增大”“减小”或“不变”)___________。
(3)C中被腐蚀的金属是___________,总反应为___________________________________。
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是__________(用A、B、C填空)。
(1)Fe+2H+====Fe2++H2↑ (2)2H++2e-====H2↑ 增大 (3)Zn Zn+2H+====Zn2++H2↑ (4)B>A>C
解析:原电池中的负极,总是较活泼的金属或易失电子的其他物质。B中活泼性Fe>Sn,故Fe为负极,Sn为正极,电极反应为:
Fe极(负极):Fe-2e-====Fe2+
Sn极(正极):2H++2e-====H2↑
C中Zn为负极,Fe为正极,Fe被保护。故Fe被腐蚀的速率为B>A>C。

练习册系列答案
相关题目