题目内容
|
空气中CO、NO、NO2、SO2都能使人中毒,其中易与人体中的血红蛋白失去运载O2和CO2能力的是 | |
A. |
CO |
B. |
NO |
C. |
NO2 |
D. |
SO2 |
答案:AB

练习册系列答案
相关题目
 乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放.但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题.
乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放.但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题.(1)NOx排入空气中,形成酸雨,造成空气污染.NOx中有一种红棕色气体,其溶于水的方程式是
(2)已知NO2和N2O4的结构式分别是
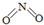 和
和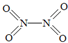 .
.| 物质 | NO2 | N2O4 | |
| 化学键 | N=O | N-N | N=O |
| 键能(kJ/mol) | 466 | 167 | 438 |
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放.
①写出用CO还原NO生成N2的化学方程式
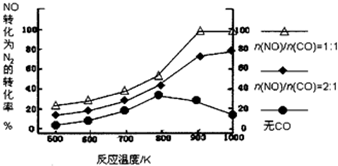
②在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和
| n(NO) |
| n(CO) |
为达到NO转化为N2的最佳转化率,应该选用的温度和
| n(NO) |
| n(CO) |
(4)用CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质.CH4与NO发生反应的化学方程式为
