题目内容
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收Na2Cr2O7等物质。

已知:水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
(1)水浸后的溶液呈____性(“酸”、“碱”、“中”)。
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式:
____Cr(OH)3+____Na2CO3+_____
 = ____Na2CrO4+___CO2+_____
= ____Na2CrO4+___CO2+_____
(3)滤渣II的主要成分有Zn(OH)2、___________________________________。
(4)“系列操作”中为:继续加入H2SO4,________冷却结晶,过滤。继续加入H2SO4目的是________________________。
已知:①除去滤渣II后,溶液中存在如下反应:2CrO42ˉ+2H+ Cr2O72ˉ+H2O
Cr2O72ˉ+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
|
温度 化学式 |
20℃ |
60℃ |
100℃ |
|
Na2SO4 |
19.5 |
45.3 |
42.5 |
|
Na2Cr2O7 |
183 |
269 |
415 |
|
Na2CrO4 |
84 |
115 |
126 |
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式____________________________。
(16分)(1)碱性 (2分)
(2)4Cr(OH)3+4Na2CO3+3O2==4Na2CrO4+4CO2+6H2O(每种物质1分,配平2分,共4分)
(3)Al(OH)3(2分)
(4)蒸发浓缩(2分) 促进平衡2CrO42ˉ+2H+ Cr2O72ˉ+H2O向正反应方向移动,尽可能生成更多溶解度更大的Na2Cr2O7(3分)
Cr2O72ˉ+H2O向正反应方向移动,尽可能生成更多溶解度更大的Na2Cr2O7(3分)
(5)CrO42ˉ+8H++6eˉ=Cr+4H2O(3分)
【解析】
试题分析:(1)碳酸钠、偏铝酸钠等是强碱弱酸盐,溶于水时能够水解,所得溶液呈碱性;(2)观察可知,铬元素由+3升为+6价,氢氧化铬作还原剂,则4Cr(OH)3+4Na2CO3+3O2==4Na2CrO4+4CO2+6H2O;(3)观察流程图,滤渣I的成分说明水浸过滤除去铜、镍,由于目标产物含铬,则加入硫酸调节pH的目的是除去锌、铝,因此推断滤渣II的主要成分是氢氧化锌、氢氧化铝;(4)根据混合物分离提纯的原理和方法推断,冷却结晶之前的操作为蒸发浓缩;由于硫酸具有酸性,铬酸根离子在溶液中存在如下平衡:2CrO42ˉ+2H+ Cr2O72ˉ+H2O,继续加入硫酸,使上述平衡右移,生成更多的重铬酸钠;根据溶解度表可知,重铬酸钠的溶解度随温度下降明显减小,因此蒸发浓缩、冷却结晶、过滤得到的滤渣III为重铬酸钠,滤液的主要成分硫酸钠和重铬酸钠;(5)铬元素由+6降为0价,发生还原反应,则该反应在阴极上发生,主要反应物和产物为CrO42ˉ→Cr;由于化合价降低总数等于得电子数,则CrO42ˉ+6eˉ→Cr;由于硫酸显酸性,应用氢离子使左右电荷守恒,则CrO42ˉ+6eˉ+8H+→Cr;根据原子个数守恒,阴极反应式为CrO42ˉ+6eˉ+8H+==Cr+4H2O。
Cr2O72ˉ+H2O,继续加入硫酸,使上述平衡右移,生成更多的重铬酸钠;根据溶解度表可知,重铬酸钠的溶解度随温度下降明显减小,因此蒸发浓缩、冷却结晶、过滤得到的滤渣III为重铬酸钠,滤液的主要成分硫酸钠和重铬酸钠;(5)铬元素由+6降为0价,发生还原反应,则该反应在阴极上发生,主要反应物和产物为CrO42ˉ→Cr;由于化合价降低总数等于得电子数,则CrO42ˉ+6eˉ→Cr;由于硫酸显酸性,应用氢离子使左右电荷守恒,则CrO42ˉ+6eˉ+8H+→Cr;根据原子个数守恒,阴极反应式为CrO42ˉ+6eˉ+8H+==Cr+4H2O。
考点:考查有关物质制备的化学工艺流程大题,涉及盐类的水解规律、氧化还原反应方程式的配平、除杂原理及滤渣成分推断、混合物分离提纯的方法、应用化学平衡移动原理解析加入硫酸的目的、阴极反应式的书写等。

 全程金卷系列答案
全程金卷系列答案铬及其化合物在现代工业上的应用广泛,可用于电镀,鞣制羊毛,皮革;铬还用于照相材料,胶版印刷及化工触媒剂等。但化工废料铬渣对人体健康有很大危害。
Ⅰ:某工厂对制革工业污泥中Cr(III)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
|
阳离子 |
Fe3+ |
Fe2+ |
Mg2+ |
Al3+ |
Cu2+ |
Cr3+ |
|
开始沉淀时的pH |
1.9 |
7.0 |
—— |
—— |
4.7 |
—— |
|
沉淀完全时的pH |
3.2 |
9.0 |
11.1 |
8 |
6.7 |
9 (>9溶解) |
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL 4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需 。
(2)酸浸时,为了提高浸取率可采取的措施是 (至少答一点)。
(3)调节溶液的pH=8是为了除去 离子。钠离子交换树脂的原理为:
Mn++nNaR→MRn+nNa+,被交换的的杂质离子是 。
(4)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH) 的溶度积Ksp= c(Cr3+)• c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
。
的溶度积Ksp= c(Cr3+)• c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
。
(5)还原过程发生以下反应(请配平): Na2Cr2O7+ SO2+
= Cr(OH) (H2O)5SO4+ Na2SO4;
Ⅱ:工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。
其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。用Fe做电极的原因为
在阴极附近溶液pH升高的原因是(用电极反应解释) 。
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧-钠氧化法”回收Na2Cr2O7等物质.

已知:水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
(1)水浸后的溶液呈______性(“酸”、“碱”、“中”)
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式
______Cr(OH)3+______Na2CO3+______=______Na2CrO4+______CO2+______
(3)滤渣II的主要成分有Zn(OH)2、______
(4)“系列操作”中为:继续加入H2SO4,______冷却结晶,过滤.继续加入H2SO4目的是______.
已知:①除去滤渣II后,溶液中存在如下反应: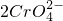 +2H+=
+2H+=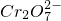 +H2O
+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
| 温度 化学式 | 20℃ | 60℃ | 100℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
