题目内容
将平均摩尔质量为8.5g/mol的N2和H2的混合气体投入恒温恒压容器中,反应达平衡时,气体体积减少40%,求①投入的N2和H2的体积比;
②N2的转化率.
【答案】分析:①利用十字交叉法计算.
②设N2和H2投入量分别为1和3mol,反应的N2为xmol,利用三段式解题法求出反应混合物各组分的物质的量的变化量、平衡时各组分的物质的量,列方程求x的值,再根据转化率的定义计算.
解答:解:①利用十字交叉法计算投入的N2和H2的体积比:
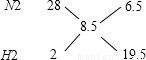
所以N2和H2的体积比为 6.5:19.5=1:3.
答:N2和H2的体积比为1:3.
②设N2和H2投入量分别为1和3mol,反应的N2为xmol,则
N2 +3H2 2NH3
2NH3
开始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
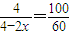 ,解得x=0.8mol
,解得x=0.8mol
所以α(N2)=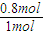 ×100%=80%.
×100%=80%.
答:N2的转化率80%.
点评:本题考查化学平衡的有关计算,难度不大,注意基础知识的积累,掌握化学平衡三段式解题法.十字交叉法运用简化计算,注意理解.
②设N2和H2投入量分别为1和3mol,反应的N2为xmol,利用三段式解题法求出反应混合物各组分的物质的量的变化量、平衡时各组分的物质的量,列方程求x的值,再根据转化率的定义计算.
解答:解:①利用十字交叉法计算投入的N2和H2的体积比:
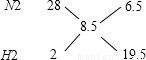
所以N2和H2的体积比为 6.5:19.5=1:3.
答:N2和H2的体积比为1:3.
②设N2和H2投入量分别为1和3mol,反应的N2为xmol,则
N2 +3H2
 2NH3
2NH3开始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
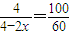 ,解得x=0.8mol
,解得x=0.8mol所以α(N2)=
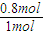 ×100%=80%.
×100%=80%.答:N2的转化率80%.
点评:本题考查化学平衡的有关计算,难度不大,注意基础知识的积累,掌握化学平衡三段式解题法.十字交叉法运用简化计算,注意理解.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
 在100℃时,将0.4mol的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
在100℃时,将0.4mol的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据: N2O4的平衡常数将
N2O4的平衡常数将 N2O4将
N2O4将