题目内容
C6H12O、 C3H6O、 C5H10O组成的混合物1.75g在足量氧气中充分燃烧后生成1.8g水,则三种有机物的平均相对分子质量为( )
A.86 B. 80 C. 78 D. 72
B
解析:根据分子式可知,碳和氢的原子个数之比是1︰2的,质量之比是6︰1。水是1.8g,则 原子的质量是0.2g,因此原混合物中碳的质量就是1.2g。所以氧原子的质量是1.75g-0.2g-1.2g=0.35g,因为每一种物质中都含有1个氧原子,所以混合物的平均相对分子质量为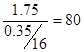 ,所以正确的答案是B。
,所以正确的答案是B。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
工业上合成氨的原料之一为氢气,其来源之一是利用石油气的有关成分如丙烷(C3H8)制取.以下途径,假设反应都能进行,则从经济效益考虑最合理的反应是( )
A、C3H8
| ||||
B、C3H8
| ||||
C、C3H8+6H2O
| ||||
D、2H2O
|
根据图判断,下列说法不正确的是( )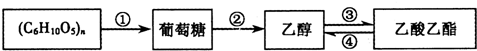

| A、(C6H10O5)n可表示淀粉或纤维素 | ||
B、反应②化学方程式为C6H12O
| ||
| C、反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去 | ||
| D、反应③和④都属于取代反应 |
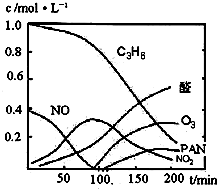 汽车尾气已经成为大气污染的主要污染源之一,某探究性学习小组的同学在一次社会实践中,到环保部门做了烟雾箱实验,他们起始时投入丙烯、NO及空气,用紫外线长时间照射气体,发生了一系列变化,用物质感应器数据采集器,通过计算机得出如图所示的变化曲线.结合曲线,试回答下列问题.
汽车尾气已经成为大气污染的主要污染源之一,某探究性学习小组的同学在一次社会实践中,到环保部门做了烟雾箱实验,他们起始时投入丙烯、NO及空气,用紫外线长时间照射气体,发生了一系列变化,用物质感应器数据采集器,通过计算机得出如图所示的变化曲线.结合曲线,试回答下列问题.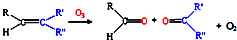 ,写出丙烯与臭氧作用生成醛的化学方程式(并配平)
,写出丙烯与臭氧作用生成醛的化学方程式(并配平)
 的名称
的名称
