题目内容
如下图装置,待内外空气压强不变时标注出水银液面的刻度(用红漆),取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞.硫粉安静地燃烧,水银柱推向左管.当火焰熄灭后静置,水银柱又慢慢回到原先标定的刻度.简要回答下列问题:
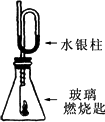
(1)水银柱推向左管说明了________.
(2)硫粉未燃尽时火焰就熄灭了,说明________.
(3)根据水银柱最后回到原先标定的刻度,可得到的结论是________.
(4)根据反应方程式S+O2![]() SO2和上述结论又可推导出(或证明)________.
SO2和上述结论又可推导出(或证明)________.
答案:
解析:
解析:
|
答案:(1)①该反应是放热反应;②气体受热膨胀 (2)瓶内氧气耗尽 (3)①同温、同压下,反应消耗的氧气与生成的SO2体积相同 ②压强相同 ③物质的量相同 (4)同温、同压下,相同体积的气体含有相同的分子数 点拨:此题的反应原理为S+O2 |

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
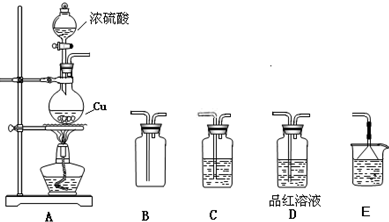
 长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来定性、定量测定亚硫酸钠试剂的被氧化的程度,设计如下方案:
长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来定性、定量测定亚硫酸钠试剂的被氧化的程度,设计如下方案: 如图装置,待内外空气压强不变时标注出水银液面的刻度(用红漆),取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞.硫粉安静地燃烧,水银柱推向左管.当火焰熄灭后静置,水银柱又慢慢回到原先标定的刻度.简要回答下列问题:
如图装置,待内外空气压强不变时标注出水银液面的刻度(用红漆),取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞.硫粉安静地燃烧,水银柱推向左管.当火焰熄灭后静置,水银柱又慢慢回到原先标定的刻度.简要回答下列问题: