题目内容
1.下列离子方程式正确的是( )| A. | 向硫酸铝溶液中滴加过量的氨水:Al3++4OH?═AlO2?+2H2O | |
| B. | 金属铜与浓硝酸反应:3Cu+8H++2NO3?═3Cu2++2NO↑+4H2O | |
| C. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl?$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
分析 A.氨水为弱碱,二者反应生成氢氧化铝沉淀;
B.铜与浓硝酸反应生成的是二氧化氮气体;
C.离子方程式两边总电荷不相等,违反了电荷守恒;
D.偏铝酸钠与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠.
解答 解:A.硫酸铝与氨水反应生成硫酸铵和氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.金属铜与浓硝酸反应生成硝酸铜、二氧化氮气体和水,正确的离子方程式为:Cu+4H++2NO3?═Cu2++2NO2↑+2H2O,故B错误;
C.实验室用浓盐酸与MnO2反应制Cl2,正确的离子方程式为:MnO2+4H++2Cl?$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O,故C错误;
D.NaAlO2溶液中通入过量CO2,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
8.下列化学用语正确的是( )
| A. | S原子的结构示意图: | |
| B. | 氯化钠的电子式: | |
| C. | 乙醇的结构式: | |
| D. | 硫酸的电离方程式:HSO4=H2++SO42- |
9.下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离; ②除去福尔马林中的乙酸,加入足量饱和碳酸钠溶液充分振荡蒸馏,收集馏出物 ③除去CO2中少量的SO2;气体通过盛有饱和碳酸钠溶液的洗气瓶; ④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离; ②除去福尔马林中的乙酸,加入足量饱和碳酸钠溶液充分振荡蒸馏,收集馏出物 ③除去CO2中少量的SO2;气体通过盛有饱和碳酸钠溶液的洗气瓶; ④除去乙醇中少量的乙酸:加足量生石灰,蒸馏.
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
13.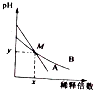 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示,下列说法正确的是( )| A. | 稀释前,c(A)=10c(B) | |
| B. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 | |
| C. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7mol/L | |
| D. | 由图可知,A为强碱,B为弱碱 |
10.用NA表示阿伏加德罗常数,则下列说法正确是( )
| A. | 常温常压下,11.2L CH4中含有的氢原子数为2NA | |
| B. | 11.2 L CO2与8.5 g NH3所含分子数相等 | |
| C. | 常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 常温下,1L 0.1mol/L MgCl2溶液中含Cl- 数为0.1NA |
11.下列有关仪器的使用方法或实验操作正确的是( )
| A. | 做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶 | |
| B. | 酸式滴定管装标准液前,必须先用该溶液润洗 | |
| C. | 锥形瓶用作反应容器时一定不能加热 | |
| D. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体 |



