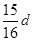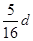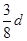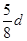题目内容
下列溶液中NO3-的浓度与500 mL 0.4 mol·L-1 KNO3溶液中NO3-的浓度相等的是
| A.50 mL 4 mol·L-1的KNO3溶液 |
| B.1 L 0.2 mol·L-1的KNO3溶液 |
| C.100 mL 0.2 mol·L-1的Ba(NO3)2溶液 |
| D.500 mL 0.4 mol·L-1的Ba(NO3)2溶液 |
C
解析

练习册系列答案
相关题目
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A.H2O的电子式: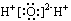 |
B.质量数为14的碳原子: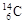 |
C.CO2的比例模型: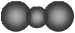 |
D.Cl-的结构示意图: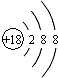 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,2.24 L H2O所含分子数为0.1NA |
| B.常温常压下,500 mL 0.1mol/L醋酸溶液中含有分子的总数目为0.05NA |
| C.78g Na2O2固体中Na+的数目为2NA |
| D.5.6 g铁与足量盐酸反应转移的电子数为0.3NA |
下列化学用语正确的是( )
A.聚丙烯的结构简式: |
B.四氯化碳分子的电子式: |
C.2-乙基-1,3-丁二烯分子的键线式: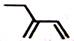 |
D.丙烷分子的比例模型: |
在下列条件下,两瓶气体所含的原子数一定相等的是( )
| A.具有同压强、同体积的N2O和CO2 |
| B.具有同温度、同体积的CO和N2 |
| C.具有同体积、同密度的SO2和NO2 |
| D.具有同质量、不同密度的O2和O3 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+,取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中
| A.至少存在5种离子 |
| B.Cl-一定存在,且c(Cl?)≥0.4mol/L |
| C.SO42-、NH4+、一定存在,Cl-可能不存在 |
| D.CO32-、Al3+一定不存在,K+可能存在 |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有4nA个电子 |
| B.1L0.1mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4L盐酸含有nA个HCl分子 |
| D.1molNa被完全氧化生成Na2O2,失去个2nA电子 |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |