题目内容
16.下列各组元素性质递变的情况中,错误的是( )| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高化合价依次升高 | |
| C. | N、O、F原子半径依次增大 | |
| D. | P、S、Cl元素的最低化合价依次为-3、-2、-1 |
分析 A.Li、Be、B原子最外层电子数分别为1、2、3;
B.P、S、Cl元素最高化合价分别为+5、+6、+7;
C.同周期从左向右原子半径减小;
D.元素的最低化合价等于最外层电子数-8.
解答 解:A.Li、Be、B原子最外层电子数分别为1、2、3,则最外层电子数依次增多,故A正确;
B.P、S、Cl元素最高化合价分别为+5、+6、+7,则最高化合价依次升高,故B正确;
C.同周期从左向右原子半径减小,则N、O、F原子半径依次减小,故C错误;
D.P、S、Cl元素的最低化合价分别为5-8=-3、6-8=-2、7-8=-1,则P、S、Cl元素的最低化合价依次为-3、-2、-1,故D正确;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
7.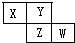 X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )| A. | Z元素的氧化物对应的水化物是强酸 | |
| B. | 含有X、Y、Z的化合物一定是共价化合物 | |
| C. | X的气态氢化物与W的气态氢化物反应的生成物中一定含有离子 | |
| D. | 原子半径大小顺序:X>Y>Z>W |
4.为提纯下列物质(括号内为杂质),所选用的试剂和分离方法均正确的是( )
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | 乙醇 (乙酸) | NaOH溶液 | 蒸馏 |
| B | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 溴乙烷(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
8.m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4.将反应后的混合气体完全燃烧生成CO2和H2O,所需要氧气的物质的量是( )
| A. | (3m+n)mol | B. | ($\frac{5}{2}$m+$\frac{n}{2}$-3p)mol | C. | (3m+n+2p)mol | D. | ($\frac{5}{2}$m+$\frac{n}{2}$)mol |
5.HgCl2的稀溶液可用作手术刀的消毒剂,已知HgCl2的熔点是2770C,熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力,则下列关于的叙述正确的是( )
| A. | HgCl2 属于共价化合物 | B. | HgCl2 属于离子化合物 | ||
| C. | HgCl2 属于非电解质 | D. | HgCl2属于强电解质 |
6.化学反应前后一定发生变化的是( )
| A. | 原子个数 | B. | 化学键 | C. | 质量 | D. | 元素种类 |
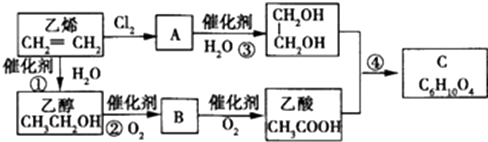
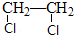 .
.
 .
. ;G的结构简式
;G的结构简式 .F1和F2互为同分异构体.
.F1和F2互为同分异构体.