题目内容
6.下列实验操作正确的是( )| A. | 用碱式滴定管量取10.00mL 1mol•L-1的KMnO4溶液 | |
| B. | 酸碱中和滴定时锥形瓶在滴定前用待测液润洗2~3次 | |
| C. | 含有Mg(OH)2和Ca(OH)2的浊液中加入足量MgCl2,充分反应后过滤可除去Ca(OH)2 | |
| D. | 将一定量的氯化铁固体溶解在水中,用玻璃棒搅拌即可配得氯化铁溶液 |
分析 A.KMnO4溶液用酸式滴定管量取;
B.用待测液润洗锥形瓶,溶质增加;
C.沉淀向更难溶的方向转化;
D.氯化铁中Fe3+能发生水解.
解答 解:A.KMnO4溶液具有强氧化性,能够腐蚀碱式滴定管的橡胶管,所以不能用碱式滴定管量取的KMnO4溶液,应该用酸式滴定管,故A错误;
B.润洗后锥形瓶中会残留一些待测液,这样滴定时相当于多滴定了一些待测液,消耗的滴定剂增大,结果就偏高,故B错误;
C.由于氢氧化镁比氢氧化钙难溶,故向含有Mg(OH)2和Ca(OH)2的浊液中加入足量的MgCl2溶液,镁离子会结合氢氧根离子生成Mg(OH)2的沉淀,使Ca(OH)2不断溶解而除去,故C正确;
D.配制氯化铁溶液时,将一定量氯化铁固体溶解在较浓的盐酸中,再用水稀释到所需浓度,故D错误.
故选C.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
相关题目
14.下列各组离子中,能在溶液中大量共存的是( )
| A. | Na+、Cu2+、Cl-、OH- | B. | K+、Ca2+、HCO3-、OH- | ||
| C. | Fe2+、H+、SO42-、NO3- | D. | Na+、CO32-、OH-、K+ |
1.下列各组离子在溶液中能够大量共存的是( )
| A. | Na+、Al3+、Cl-、HCO3- | |
| B. | 使pH试纸显蓝色的溶液:K+、Cu2+、Cl-、SO42- | |
| C. | 滴入甲基橙指示剂呈红色的溶液:Na+、NH4+、ClO4-、NO3- | |
| D. | 水电离出的c(H+)=1×10-13mol/L的溶液:K+、NH4+、SO32-、Cl- |
11.短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A是原子半径最小的元素,A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍.下列叙述正确的是( )
| A. | 元素的原子半径:A<B<C<D<E | |
| B. | 对应氢化物的热稳定性:D>E | |
| C. | B与C、B与D形成的化合物中化学键类型相同 | |
| D. | 五种元素中最高价氧化物对应的水化物酸性最强的是E |
18.通常状况下,单斜硫和正交硫是硫的两种固态的同素异形体.已知热化学方程式:
①S(s,单斜)+O2(g)→SO2 (g)+297.16kJ
②S(s,正交)+O2(g)→SO2 (g)+296.83kJ
下列说法错误的是( )
①S(s,单斜)+O2(g)→SO2 (g)+297.16kJ
②S(s,正交)+O2(g)→SO2 (g)+296.83kJ
下列说法错误的是( )
| A. | 单斜硫比正交硫稳定 | |
| B. | 单斜硫转化为正交硫需要放出热量 | |
| C. | 单斜硫升华为气态时要吸收热量 | |
| D. | 将同态的硫单质气化或液化能提高它们的燃烧效率 |

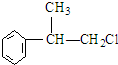 或
或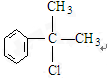 ;
;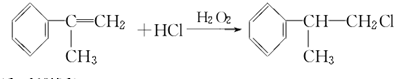 ;
;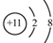 .
.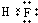 、
、 ,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.
,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.