题目内容
【题目】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布图为________。
②1 mol CH2=CH-CH2OH含有σ键的数目为________,烯丙醇分子中碳原子的杂化类型为___。
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的阴离子为_____。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为_______。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中σ键和π键数目比是________。
【答案】![]() 9NA sp2、sp3 C22-
9NA sp2、sp3 C22- ![]() 2:1
2:1
【解析】
(1)①Ni是28号元素,原子核外电子排布式为:1s22s22p63s23p63d84s2,据此判断价电子的排布图;
②单键为σ键,双键含有1个σ键、1个π键,据此分析判断CH2=CH-CH2OH分子中含有的σ键数目;分子中碳原子均没有孤电子对,而碳碳双键中碳原子形成3个σ键,杂化轨道数目为3,另外碳原子形成4个σ键,杂化轨道数目为4;
③用替代法书写等电子体;
(2)①等电子体结构和性质相似,C22-与O22+和氮气互为等电子体,根据氮气分子电子式书写O22+电子式;
②单键为σ键,双键含有1个σ键、1个π键,三键含有1个σ键、两个π键,据此分析。
(1)①Ni是28号元素,原子核外电子排布式为:1s22s22p63s23p63d84s2,价电子排布式为:3d84s2,价电子排布图为![]() 。
。
②单键为σ键,双键含有1个σ键、1个π键,CH2=CH-CH2OH分子含有9个σ键,故1molCH2=CH-CH2OH含9molσ键,即含有σ键的数目为9NA;分子中碳原子均没有孤电子对,而碳碳双键中碳原子形成3个σ键,杂化轨道数目为3,C原子的杂化方式为sp2杂化,另外碳原子形成4个σ键,杂化轨道数目为4,碳原子采取sp3杂化。
③等电子体是指价电子总数和原子总数相同的分子、离子或原子团,则与CN-互为等电子体的分子为N2或CO、阴离子为C22-。
(2)①等电子体结构和性质相似,C22-与O22+和氮气互为等电子体,根据氮气分子的电子式可知,O22+电子式为![]() 。
。
②H2C=CH-C≡N分子中含3个C—H键、1个C=C键、1个C—C键、1个C≡N键,单键为σ键,双键含有1个σ键、1个π键,三键含有1个σ键、两个π键,则丙烯腈分子中σ键和π键数目比是6:3=2:1。

【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以纯铜屑为原料制取的流程如下:
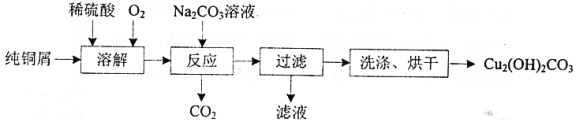
(1)“溶解”步骤反应的离子方程式为_______.温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃ ,_____
(2)“反应”步骤生成Cu2(OH)2CO3的化学方程式为_________。反应后溶液中铜元素残留量受pH和反应时间的影响如图所示:
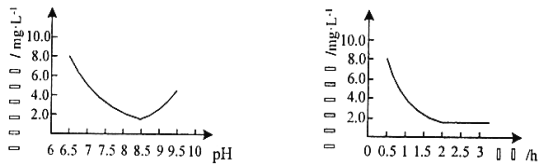
判断反应的最佳条件: pH为___、反应时间为____h。
(3)检验Cu2(OH)2CO3洗涤是否完全的方法是____________________
(4) Cu2(OH)2CO3也可以表示为CuCO3·Cu(OH)2。 查阅文献,上述反应条件下还可能生成少量CuCO3·Cu(OH)2。为测定产品的纯度[产品中Cu2(OH)2CO3的质量分数],取10.97g干燥样品,400℃左右加热,测得固体质量随时间变化关系如图所示。
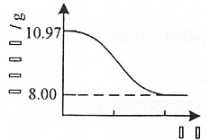
已知: 8.00g固体为黑色纯净物。
有关物质的摩尔质量如表:
物质 | CuCO3·Cu(OH)2 | CuCO3·2Cu(OH)2 | CuO |
摩尔质量/g·mol-1 | 222 | 320 | 80 |
请计算产品的纯度(写出计算过程,结果保留3位有效数字)。______