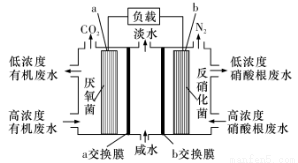
题目内容
一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高,其主要流程如下:
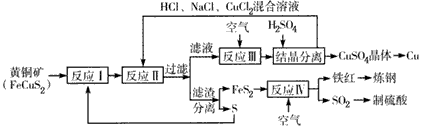
注:反应II的离子方程式为Cu2+ +CuS+4Cl- ═2[CuCl2]-+S↓
请回答下列问题;
(1)反应I的产物为 (填化学式)。
(2)反应Ⅲ的离子方程式为 。
(3)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其可能的原因是 。
(4)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均成酸性,相同条件下,同浓度的两种水溶液c(SO32-)较小的是 。
(5)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3 溶液完全反应后,用浓度为0.02000mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00Ml。 已知:Cr2O72- +Fe2+ +H+→Cr3+ +Fe3+ +H2O(未配平)反应IV所得气体中SO2的体积分数为 。
练习册系列答案
相关题目
如图是某泡腾片的标签。将这样一粒泡腾片放入水中,药片完全溶解,同时产生大量气泡。这个过程( )
泡腾片 |
每片含: 碳酸钙 500mg 维生素C 1000mg 柠檬酸 1350mg |
用量: |
用法: |
A.溶解了500mg的Ca2+
B.释放了112mL的气体
C.发生了反应:CO32- +2H+ = CO2↑+H2O
D.说明了柠檬酸的酸性比碳酸强
今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按图方式进行转化:
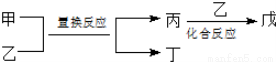
其推断正确的是
选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
A | NH3 | O2 | NO | H2O | NO2 |
B | Mg | CO2 | C | MgO | CO |
C | C | H2O | CO | H2 | C2H5OH |
D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |



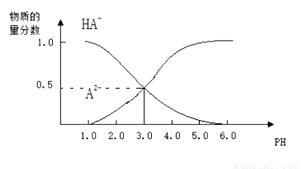
 H++HA- ,HA-
H++HA- ,HA-