题目内容
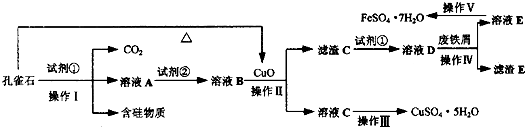
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:

请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为___ __(填代号),检验溶液A中Fe3+的最佳试剂为___ _(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、_______ _、过滤等操作。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列_____ ___(填代号)装置回收。

写出制备碳酸钙的化学方程式
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应_____ __ _ ,直到_____ _ __。用KMnO4标准溶液滴定时应选用______ __滴定管((填“酸式”或“碱式”)。
(5)已知:无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
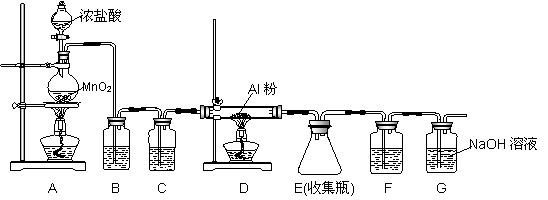

①写出A中反应的离子方程式
②装置B中盛放饱和NaCl溶液,该装置的主要作用是 。F中试剂的作用是 。用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 _。
(1)c d (2)冷却结晶 (3)NH3 (或NH3·H2O) b d (2分)
CaCl2 +2 NH3·H2O+CO2=== CaCO3↓+2NH4 Cl+H2O;(2分)
(4)注视凹液面的最低处与刻度线, 凹液面的最低处与刻度线相平 酸式
(5) ①MnO2+4H+ +Cl-![]() Mn2++Cl2↑+2H2O;(2分)
Mn2++Cl2↑+2H2O;(2分)
②除去HCl; 吸收水蒸气; 碱石灰(或NaOH与CaO混合物)
(没标分数的每空1分)

 阅读快车系列答案
阅读快车系列答案