题目内容
8.下列说法不正确的是( )| A. | 碳酸钠常用于治疗胃溃疡病人的胃酸过多症 | |
| B. | 切开的金属Na暴露在空气中,光亮表面会逐渐变暗 | |
| C. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| D. | 金属钠着火时,可以使用泡沫灭火器来灭火 |
分析 A.Na2CO3碱性太强;
B.变暗生成氧化钠;
C.碳酸氢钠受热分解出二氧化碳,使焙制出的糕点疏松多孔;
D.金属钠是一种活泼金属,用来灭火的物质和金属钠以及钠燃烧后的产物之间不能反应;
解答 解:A.Na2CO3碱性太强,不宜做胃药,故A错误;
B.切开的金属Na暴露在空气中,光亮表面逐渐变暗,发生反应为4Na+O2═2Na2O,故B正确;
C.发酵粉中含有碳酸氢钠,碳酸氢钠受热分解出二氧化碳,使焙制出的糕点疏松多孔,故C正确;
D.泡沫灭火器产生的二氧化碳能与钠燃烧后的产物过氧化钠产生氧气,氧气能助燃,所以金属钠着火时,不能使用泡沫灭火器来灭火,应用沙子扑灭,故D错误;
故选:AD;
点评 本题考查了元素化合物知识,明确各种物质的性质是解题关键,注意治疗胃酸过多用碳酸氢钠,题目难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
4.一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )

| A. | A为电源的正极 | |
| B. | 气体X是H2 | |
| C. | 电极E为阴极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-=C6H12 |
19.若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 通常状况下14gN2中含有电子的数目为7NA | |
| B. | 标准状况下,22.4L水中含有水分子的数目为NA | |
| C. | 1molFe与足量稀盐酸反应时,转移电子的数目为3NA | |
| D. | 数目为NA的一氧化碳分子和0.5mol甲烷的质量比为7:4 |
16.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴乙烷制乙烯;由石油制乙烯 | |
| B. | 由乙烯制乙烷;由乙醇制乙醛 | |
| C. | 乙烯使溴水褪色;甲苯使酸性KMnO4溶液褪色 | |
| D. | 由硝酸与苯反应制硝基苯;甲烷与Cl2光照 |
13.下列各图与表述一致的是( )
| A. |  图可以表示对某化学平衡体系改变温度后反应速率随时间的变化 图可以表示对某化学平衡体系改变温度后反应速率随时间的变化 | |
| B. |  用图所示装置蒸发AlCl3溶液制备无水AlCl3 用图所示装置蒸发AlCl3溶液制备无水AlCl3 | |
| C. |  图可以表示向一定量的明矾溶液中逐滴滴加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化 图可以表示向一定量的明矾溶液中逐滴滴加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化 | |
| D. |  图电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B 图电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B |
20.下列解释事实的方程式不正确的是( )
| A. | 醋酸溶液显酸性:CH3COOH?H++CH3COO- | |
| B. | 用氨水除去烟气中的SO2:SO2+2NH3•H2O=(NH4)2SO3+H2O | |
| C. | 向盐碱地中施放硫酸钙,降低其碱性:Na2CO3+CaSO4=CaCO3+Na2SO4 | |
| D. | 用三氯化铁溶液腐蚀线路板:Fe3++Cu=Fe2++Cu2+ |
18.下列有机物命名正确的是( )
| A. | 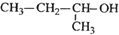 2-甲基-1-丙醇 2-甲基-1-丙醇 | B. |  3-乙基-1-丁烯 3-乙基-1-丁烯 | ||
| C. |  2-甲基-2,4-己二烯 | D. | 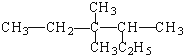 3,4,4-三甲基己烷 |
 .
.