题目内容
某废水处理厂处理废水中NH+的过程如下:
①NH4+
(aq)+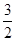 O2(g)=HNO2(aq)+H+(aq)+H2O(1)
ΔH=-b KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1)
ΔH=-b KJ/mol
②2HNO2(aq)+O2(g)=2NO3- (aq)+2H+ ΔH=-aKJ/mol
下列叙述正确的是( )
A.将NH4+转化为NO3-的热化学方程式可表示为:
NH4+ (aq)+2O2(g)=NO3-
(aq)+2H+(aq)+H2O(1) ΔH=-(b+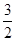 )KJ/mol
)KJ/mol
B.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
C.常温下,若HNO3溶液中c(H+)=0.1 mol·L-1,则该溶液的pH>1
D.若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)=c(NO3-)+c(H+)
【答案】
A
【解析】
试题分析:B、在上述两次转化过程中,废水的酸性一直在增大,错误;C、常温下,溶液中c(H+)=0.1 mol•L-1时,溶液的pH=1,错误;D、若上述两次转化完全,则溶液中不存在NH4+,错误。
考点:考查化学基本概念和基本理论相关知识。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目

