题目内容
短周期元素 X、Y、Z 可组成化学式为 XYZ3 的四种化合物甲、乙、丙、丁.
(l)若甲中 X 的原子只有一个质子,Y、Z同周期,画出Z的电子排布图为
 .
.
(2)若乙中X、Y、Z 三种元素的原子序数之和为 26,Y、Z 同周期,且乙是一种微溶于水的盐,并写出工业制备单质X的化学方程式:
(3)若丙中X元素的焰色反应为黄色,Y与X同周期,Y 是同周期中原子半径最小的元素,丙与浓盐酸反应生成 Y 单质的化学方程式为
(4)若丁中 X、Y、Z 处于不同周期,X的族序数是周期序数的二倍,Z原子核外电子占有9个轨道,且具有一个未成对电子,则丁的结构式为
 .
.
(l)若甲中 X 的原子只有一个质子,Y、Z同周期,画出Z的电子排布图为


(2)若乙中X、Y、Z 三种元素的原子序数之和为 26,Y、Z 同周期,且乙是一种微溶于水的盐,并写出工业制备单质X的化学方程式:
MgCl2
Mg+Cl2↑
| ||
| 熔融 |
MgCl2
Mg+Cl2↑
.
| ||
| 熔融 |
(3)若丙中X元素的焰色反应为黄色,Y与X同周期,Y 是同周期中原子半径最小的元素,丙与浓盐酸反应生成 Y 单质的化学方程式为
NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O
NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O
.(4)若丁中 X、Y、Z 处于不同周期,X的族序数是周期序数的二倍,Z原子核外电子占有9个轨道,且具有一个未成对电子,则丁的结构式为


分析:(1)X的原子只有一个质子,为H元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的化合物,在化合物中H显+1价,Y为+5价,Z是-2价,Y、Z同周期,则Y是N元素,Z是O元素;
(2)若乙中X、Y、Z 三种元素的原子序数之和为26,Y、Z 同周期,且乙是一种微溶于水的盐,且X、Y、Z是短周期元素,则乙是碳酸镁,X是镁,Y是C 元素,Z是O元素,活泼金属采用电解其熔融盐的方法冶炼;
(3)若丙中X元素的焰色反应为黄色,则X是钠元素,Y与X同周期,Y是同周期中原子半径最小的元素,则Y是Cl元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的盐,所以丙是氯酸钠,则Z是O元素,根据反应物和生成物写出反应方程式;
(4)若丁中 X、Y、Z 处于不同周期,Z原子核外电子占有9个轨道,且具有一个未成对电子,则Z是Cl元素,X的族序数是周期序数的二倍,则X是C元素,Y是H元素,则丁是三氯甲烷,根据丁的结构写出其结构式.
(2)若乙中X、Y、Z 三种元素的原子序数之和为26,Y、Z 同周期,且乙是一种微溶于水的盐,且X、Y、Z是短周期元素,则乙是碳酸镁,X是镁,Y是C 元素,Z是O元素,活泼金属采用电解其熔融盐的方法冶炼;
(3)若丙中X元素的焰色反应为黄色,则X是钠元素,Y与X同周期,Y是同周期中原子半径最小的元素,则Y是Cl元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的盐,所以丙是氯酸钠,则Z是O元素,根据反应物和生成物写出反应方程式;
(4)若丁中 X、Y、Z 处于不同周期,Z原子核外电子占有9个轨道,且具有一个未成对电子,则Z是Cl元素,X的族序数是周期序数的二倍,则X是C元素,Y是H元素,则丁是三氯甲烷,根据丁的结构写出其结构式.
解答:解:(1)X的原子只有一个质子,为H元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的化合物,在化合物中H显+1价,Y为+5价,Z是-2价,Y、Z同周期,则Y是N元素,Z是O元素,Z原子核外有8个电子,根据构造原理知,Z的电子排布图为 ,故答案为:
,故答案为: ;
;
(2)若乙中X、Y、Z 三种元素的原子序数之和为26,Y、Z 同周期,且乙是一种微溶于水的盐,且X、Y、Z是短周期元素,则乙是碳酸镁,X是镁,Y是C 元素,Z是O元素,工业上采用电解熔融氯化镁的方法冶炼镁,其反应方程式为MgCl2
Mg+Cl2↑,故答案为:MgCl2
Mg+Cl2↑;
(3)若丙中X元素的焰色反应为黄色,则X是钠元素,Y与X同周期,Y是同周期中原子半径最小的元素,则Y是Cl元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的盐,所以丙是氯酸钠,则Z是O元素,氯酸钠和浓盐酸反应生成氯化钠、氯气和水,反应方程式为:NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O,
故答案为:NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O;
(4)若丁中 X、Y、Z 处于不同周期,Z原子核外电子占有9个轨道,且具有一个未成对电子,则Z是Cl元素,X的族序数是周期序数的二倍,则X是C元素,Y是H元素,则丁是三氯甲烷,三氯甲烷是四面体结构,其结构式为 ,故答案为:
,故答案为: .
.
 ,故答案为:
,故答案为: ;
;(2)若乙中X、Y、Z 三种元素的原子序数之和为26,Y、Z 同周期,且乙是一种微溶于水的盐,且X、Y、Z是短周期元素,则乙是碳酸镁,X是镁,Y是C 元素,Z是O元素,工业上采用电解熔融氯化镁的方法冶炼镁,其反应方程式为MgCl2
| ||
| 熔融 |
| ||
| 熔融 |
(3)若丙中X元素的焰色反应为黄色,则X是钠元素,Y与X同周期,Y是同周期中原子半径最小的元素,则Y是Cl元素,短周期元素 X、Y、Z 可组成化学式为 XYZ3 的盐,所以丙是氯酸钠,则Z是O元素,氯酸钠和浓盐酸反应生成氯化钠、氯气和水,反应方程式为:NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O,
故答案为:NaClO3+6HCl(浓)=3Cl2↑+NaCl+3H2O;
(4)若丁中 X、Y、Z 处于不同周期,Z原子核外电子占有9个轨道,且具有一个未成对电子,则Z是Cl元素,X的族序数是周期序数的二倍,则X是C元素,Y是H元素,则丁是三氯甲烷,三氯甲烷是四面体结构,其结构式为
 ,故答案为:
,故答案为: .
.点评:本题考查位置结构及其关系,正确推断元素是解本题的关键,充分利用所给信息进行分析判断,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
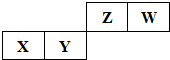 短周期元素X、Y、Z、W在周期表的位置如图所示,其中X元素所处的周期序数与族序数相等.下列判断正确的是( )
短周期元素X、Y、Z、W在周期表的位置如图所示,其中X元素所处的周期序数与族序数相等.下列判断正确的是( )| A、气态氢化物的稳定性:Y>Z | B、一定条件下,Z单质与W的常见单质直接反应生成ZW2 | C、原子半径:X>Y>Z>W | D、Y、Z的最高价氧化物均为共价化合物 |
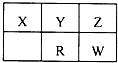 短周期元素X、Y、Z、R和W在元素周期表的位置如图所示,其中W元素族序数等于周期序数的2倍.则下列说法正确的是( )
短周期元素X、Y、Z、R和W在元素周期表的位置如图所示,其中W元素族序数等于周期序数的2倍.则下列说法正确的是( )| A、原子半径从小到大:X<Y<R<W | B、Z、W元素与X均可以形成AB2型化合物 | C、X有多种同素异形体,而Z不存在同素异形体 | D、Z的氢化物稳定性大于W的氢化物稳定性,是因为Z的氢化物分子间存在氢键 |
 短周期元素X、Y、Z关系如图,X原子的电子层数为n,最外层电子数为2n.W原子最内层电子数是最外层电子数的2倍.下列说法错误的是( )
短周期元素X、Y、Z关系如图,X原子的电子层数为n,最外层电子数为2n.W原子最内层电子数是最外层电子数的2倍.下列说法错误的是( )| A、X 和Y都是非金属元素,其中X最高化合价为+5价 | B、X、W的最高价氧化物在一定条件下能反应 | C、元素X、W和氧元素可形成化学式为W2XO3共价化合物 | D、Y、Z的氢化物的稳定性:Y<Z |


