题目内容
(14分)下表所示的是第二周期元素中,除Be、B、Ne三种元素外,其它元素的简单氢化物的沸点;题26图所示是第三周期元素中,除Ar以外的其它元素的单质的熔点变化关系。


(1)X的简单氢化物属于 分子(填“极性”或“非极性”),G元素的单质在固态时的晶体类型为___ _。
(2)写出W的氢化物的电子式 ______。
(3)A和Z两元素形成的一种化合物分子中各原子最外均达到8电子稳定结构,则该分子的结构式为 。
(4)化合物AY能与水反应生成两种弱酸,其化学方程式为
(5)写出元素F的单质与三氧化二铬反应的化学方程式___
(1)极性 (2分),原子晶体(2分) (2)Li+[:H]-(2分)
(3) 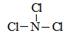 (2分)
(4)ClF+H2O=HClO+HF(3分)
(2分)
(4)ClF+H2O=HClO+HF(3分)
(5)2Al+Cr2O3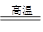 Al2O3+2Cr(3分)
Al2O3+2Cr(3分)
【解析】(1)X的氢化物的沸点是100℃,所以X是水,属于极性分子。G单质的熔点最高,应该是单质硅,属于原子晶体。
(2)W的氢化物最高,应该是离子化合物,而在第二周期中能析出离子晶体的是LiH,电子式为Li+[:H]-。
(3)A的熔点最低,应该是氯气。Z的氢化物沸点仅比M的氢化物沸点高,所以Z是氮元素。由于化合物分子中各原子最外均达到8电子稳定结构,所以是NCl3,结构类似于氨气,所以结构式为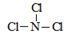 。
。
(4)Y是F,非金属性最强,所以ClF和水反应的方程式为ClF+H2O=HClO+HF。
(5)F单质的熔点仅比硅的底,所以F是铝。发生铝热反应,反应式为2Al+Cr2O3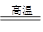 Al2O3+2Cr。
Al2O3+2Cr。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案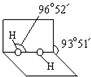 (1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是(2)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
(4)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:R3+
| OH- |
| H+ |
| ||
| H+ |
①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键.


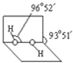 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取

