题目内容
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,则
- A.原子半径:丁>丙>乙>甲
- B.单质的还原性:丁>丙>甲
- C.甲、乙、丙的氧化物均为共价化合物
- D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
D
甲和乙形成的气态化合物的水溶液呈碱性,说明甲是H,乙是N,形成的混合物是氨气。甲和丙同主族,且丙的原子序数大于N的,所以丙是Na。丁的原子序数大于Na的,又因为丁原子最外层电子数与电子层数相等,所以丁是Al。同主族自上而下原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。所以原子半径是丙>丁>乙>甲,A不正确。单质的还原性是丙>丁>甲,B不正确。钠是活泼的金属,氧化物是离子化合物,C不正确。氢氧化铝是两性氢氧化物,既能溶于氢氧化钠中,也能溶于硝酸中,D正确。答案选D。
甲和乙形成的气态化合物的水溶液呈碱性,说明甲是H,乙是N,形成的混合物是氨气。甲和丙同主族,且丙的原子序数大于N的,所以丙是Na。丁的原子序数大于Na的,又因为丁原子最外层电子数与电子层数相等,所以丁是Al。同主族自上而下原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。所以原子半径是丙>丁>乙>甲,A不正确。单质的还原性是丙>丁>甲,B不正确。钠是活泼的金属,氧化物是离子化合物,C不正确。氢氧化铝是两性氢氧化物,既能溶于氢氧化钠中,也能溶于硝酸中,D正确。答案选D。

练习册系列答案
相关题目
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,它们的部分化合价如下表,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 最高正价或最低负价 | -4 | +1 | +4 | -2 | -1 |
| A、乙的单质中能与水剧烈反应 |
| B、气态氢化物的稳定性:丙>甲 |
| C、丙的氧化物能与戊的氢化物水溶液反应 |
| D、其最高价氧化物对应的水化物的酸性:丁>戊 |
短周期元素甲、乙、丙、丁在元素周期表的相对位置如表所示,其中甲的气态氢化物的水溶液呈碱性,则下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 |
| A、甲位于元素周期表中第2周期、第ⅤA族 |
| B、原子半径:甲>乙 |
| C、单质的氧化性:丙>乙 |
| D、气态氢化物稳定性:丁>丙>乙 |
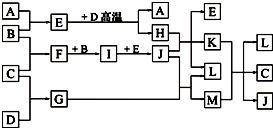 如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去).
如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去).