题目内容
下列离子方程式正确的是
| A.用Fe除去FeCl2溶液中的少量的FeCl3杂质:Fe+Fe3+=2Fe2+ |
B.实验室制取NO2:Cu+4H++2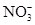 =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
C.硫酸溶液与氢氧化钡溶液混合:H++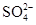 +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
D.向氯化铝溶液通足量氨气:Al3++4NH3+4H2O=4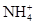 +[Al(OH)4]- +[Al(OH)4]- |
B
解析试题分析:A.电荷不守恒,正确是应该是Fe+2Fe3+=3Fe2+.错误。B.反应原理正确,拆写符合要求。正确。C.不符合客观实际。应该为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O。错误。D.一水合氨是弱碱,不能溶解氢氧化铝。应该为Al3++3NH3+3H2O=3 NH4++Al(OH)3↓.
考点:考查离子方程式的书写的知识。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
下列离子反应方程式正确的是
| A.金属钠投入蒸馏水2 Na+2H2O=2 Na++2OH- +H2↑ |
| B.向亚硫酸钠溶液中加入足量硝酸SO3 2- +2 H+=SO2↑+ H2O |
| C.用浓盐酸与MnO2反应制取少量氯气MnO2+4H++2C1- = Mn2+ + 2H2O+Cl2↑ |
| D.硫酸亚铁溶液中加入酸化的双氧水Fe2++2H++H2O2 = Fe3++2H2O |
在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,反应完全后,离子数目几乎没有变化的是
| A.Fe3+ | B.Fe2+ | C.Al3+ | D.NH4+ |
常温下,在c(H+)/c(OH?)=1×1012的溶液中,下列各组离子能大量共存的是
| A.Fe2+、Mg2+、NO3?、SO42? | B.Fe3+、Na+、Cl?、SCN? |
| C.NH4+、Al3+、NO3?、Cl? | D.Ca2+、K+、Cl?、HCO3? |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- |
| B.加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C.0.1 mol·L-1NaAlO2溶液:Al3+、Na+、Cl-、NO3- |
| D.水电离出的c(H+)=10-12 mol·L-1的溶液:Na+、K+、NH4+、CO32- |
下列溶液中的反应能用离子方程式H++OH-= H2O表示的是
| A.2NaOH+CO2=Na2CO3+H2O | B.NH3·H2O+HCl =NH4Cl+H2O |
| C.Mg(OH)2+2HCl =MgCl2+H2O | D.2KOH+H2SO4=K2SO4+2H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.无色溶液中:K+、Fe3+、SO42-、SCN- |
| C.c (H+)/c (OH-) = 1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.由水电离的c (H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
下列离子方程式正确的是( )
| A.乙酸与碳酸钠溶液反应:2H++CO32-== CO2↑+H2O |
| B.澄清石灰水中加入过量的碳酸氢钠溶液:Ca2+ + HCO + OH-= CaCO3↓ + H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O 2C6H5OH+CO32- 2C6H5OH+CO32- |
D.甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH- CO32-+2NH4++ 4Ag↓+ 6NH3↑+ 2H2O 。 CO32-+2NH4++ 4Ag↓+ 6NH3↑+ 2H2O 。 |
将以下4份溶液分别置于下图的装置中,其它条件相同时,灯泡最亮的是
| A.100mL 1mol/L的盐酸 |
| B.100mL 2mol/L的蔗糖溶液 |
| C.100mL 1mol/L的醋酸溶液 |
| D.30mL 1mol/L的CaCl2溶液 |