题目内容
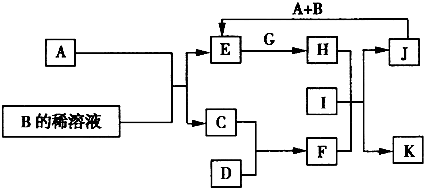
将一定量的![]() 气体通入500mL某
气体通入500mL某![]() 溶液中,充分反应后,将溶液在低温下蒸发,得到不含结晶水的白色固体A.取三份质量不同的A样品分别与50mL相同浓度的盐酸反应,得到的气体在标准状况下的体积与固体A的质量关系如下表所示:
溶液中,充分反应后,将溶液在低温下蒸发,得到不含结晶水的白色固体A.取三份质量不同的A样品分别与50mL相同浓度的盐酸反应,得到的气体在标准状况下的体积与固体A的质量关系如下表所示:
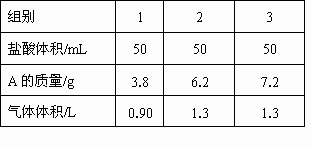
(1)从表中第________组数据表明加入的50mL盐酸反应后剩余,理由是________.
(2)试求A是什么物质,其成份的质量分数各为多少?
答案:
解析:
解析:
|
答案: (1)1同样是50mL盐酸,第1组中A的质量为3.8g,放出的气体0.90L为最少,表明该组中盐酸有余 (2)A是
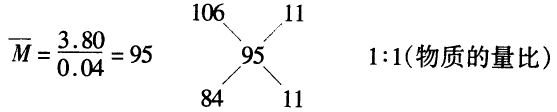
解析: 假设 假设 而实际固体的质量为3.80g,介于3.36g~4.24g之间,所以,固体为
因此,各物质的质量分数为:
|

练习册系列答案
相关题目
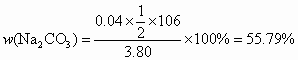 ,
, 或HC≡CH+2Br2→
或HC≡CH+2Br2→