题目内容
(9分)在体积为2L的密闭容器中发生2SO2+O2
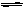 2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
(1)问:开始时,正反应速率最快的是_________;正反应速率最慢的是_________。
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(L·min),则10min时,生成的SO3浓度为 。
【答案】
(1)②;③,(2)4 mol·L-1
【解析】考查外界条件对反应速率的影响。温度越高,反应物的浓度越大,反应速率越快,所以正反应速率最快的是②,最慢的是③。
(2)根据SO2的反应速率可知,消耗SO2是0.4mol/(L·min)×10min=4mol/L,因此根据方程式可知生成三氧化硫的浓度是4mol/L。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
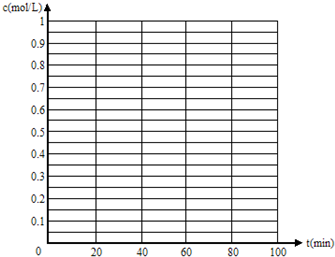
 Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:
Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答: