��Ŀ����
����Ŀ����ҵ�ϣ���500��600�����м��ͨ������������ˮ�Ȼ������������м��ͨ���Ȼ���������ˮ�Ȼ�������������ͼ��ʾ��װ��ģ���������̽������飮�ش��������⣺ 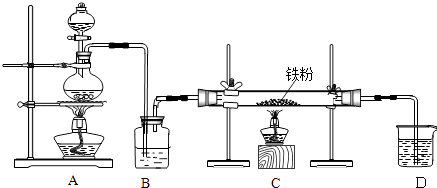
��1����ȡ��ˮ�Ȼ�����ʵ���У�A�з�Ӧ�Ļ�ѧ����ʽΪ �� װ��B�м�����Լ��� ��
��2����ȡ��ˮ�Ȼ�������ʵ���У�װ��A������ȡ �� β���ijɷ��� �� ������D��װ�ý���β�����������ڵ��������� ��
��3���������������Ƶõ�FeCl2 �Ậ������FeCl3 �� ����FeCl3���õ��Լ��� �� ���Ƶô�����FeCl2 �� ��ʵ�������Ӧ�ȵ�ȼ���ľƾ��ƣ�Ŀ���� ��
���𰸡�
��1��MnO2+4HCl��Ũ�� ![]() ?MnCl2+Cl2��+2H2O��Ũ����
?MnCl2+Cl2��+2H2O��Ũ����
��2��HCl��HCl��H2��������������ȼ������H2���ܱ�����
��3��KSCN��Һ��A���ų�װ���еĿ�������ֹ�ڼ���ʱFe��O2��Ӧ
���������⣺��1����ȡ��ˮ�Ȼ�����ʵ���У�Aװ����ȡ����������ʵ���ҳ���Ũ������������̼�����ȡ����ѧ��Ӧ����ʽΪ��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O����ȡ�������к���ˮ������װ��B�������Ǹ�������������Ũ���ᣬ���Դ��ǣ�MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O����ȡ�������к���ˮ������װ��B�������Ǹ�������������Ũ���ᣬ���Դ��ǣ�MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O��Ũ�����2����ȡ��ˮ�Ȼ���������ҪHCl���壬��Aװ����ȡ����HCl����Ӧ����ʽΪ��Fe+2HCl
MnCl2+Cl2��+2H2O��Ũ�����2����ȡ��ˮ�Ȼ���������ҪHCl���壬��Aװ����ȡ����HCl����Ӧ����ʽΪ��Fe+2HCl ![]() FeCl2+H2 �� ��β���ijɷ�Ϊδ��Ӧ��HCl�����ɵ�����������HCl��������ˮ��������Ȼ����Dװ�ý���β����������������ɵ�����������������ˮ�����������������գ�������ȼ����ɰ�ȫ���������Դ��ǣ�HCl��HCl��H2��������������ȼ������H2���ܱ����գ���3�������Ȼ����������軯����Һ����Ҫ��ȡ������FeCl2 �� �����ž�װ���еĿ�������ֹ�ڼ���ʱFe��O2��Ӧ�����ȵ�ȼA���ľƾ��ƣ��ٵ�ȼC���ľƾ��ƣ����Դ��ǣ�KSCN��Һ��A���ų�װ���еĿ�������ֹ�ڼ���ʱFe��O2��Ӧ��
FeCl2+H2 �� ��β���ijɷ�Ϊδ��Ӧ��HCl�����ɵ�����������HCl��������ˮ��������Ȼ����Dװ�ý���β����������������ɵ�����������������ˮ�����������������գ�������ȼ����ɰ�ȫ���������Դ��ǣ�HCl��HCl��H2��������������ȼ������H2���ܱ����գ���3�������Ȼ����������軯����Һ����Ҫ��ȡ������FeCl2 �� �����ž�װ���еĿ�������ֹ�ڼ���ʱFe��O2��Ӧ�����ȵ�ȼA���ľƾ��ƣ��ٵ�ȼC���ľƾ��ƣ����Դ��ǣ�KSCN��Һ��A���ų�װ���еĿ�������ֹ�ڼ���ʱFe��O2��Ӧ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ������ͼ������������̽�����������ʡ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ����������һ������������档�±��ж�ʵ�����������Ľ�����ȷ����(����)

ѡ�� | ʵ������ | �⡡�� |
A | Ũ���ḽ���������� | NH3��Ũ���ᷴӦ������С��NH4Cl���� |
B | Ũ���ḽ������������ | NH3��Ũ���������Ӧ���� |
C | �Ȼ�����Һ����� | ����Һһ����AlCl3��Һ |
D | ʪ��ĺ�ɫʯ����ֽ���� | NH3��һ�ֿ����Լ� |
A. A B. B C. C D. D
