题目内容
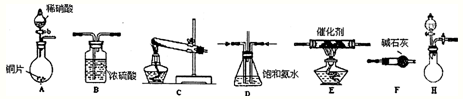
下面是实验室可制取氨气的装置和选用的试剂,其中正确的是( )
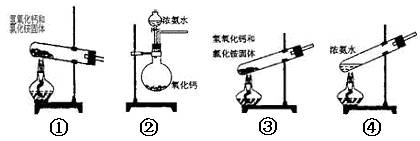
A.①③④ B.只有③ C. ①② D. ①②④
D
解析:
①可以制取氨气;②在氨水中存在平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,依据化学平衡移动原理,氧化钙与水反应放出大量热温度升高,使氨的溶解度减小而放出;氧化钙与水反应消耗水,促使氨放出;氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;③中试管口应略向下倾斜;④在氨水中存在平衡:NH3+H2O
NH4++OH-,依据化学平衡移动原理,氧化钙与水反应放出大量热温度升高,使氨的溶解度减小而放出;氧化钙与水反应消耗水,促使氨放出;氢氧化钙电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;③中试管口应略向下倾斜;④在氨水中存在平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,加热使温度升高,使氨的溶解度减小而放出。故正确的选项为D项。
NH4++OH-,加热使温度升高,使氨的溶解度减小而放出。故正确的选项为D项。

 阅读快车系列答案
阅读快车系列答案(15分)(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO 2CO2+N2
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 | T/℃ | NO初始浓度 mol·L-1 | CO初始浓度 mol·L-1 | 催化剂的比表面积 ㎡·g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ |
|
|
| 124 |
| Ⅲ | 350 |
|
| 124 |
①请在表格中填入剩余的实验条件数据。
②设计实验Ⅱ、Ⅲ的目的是 。
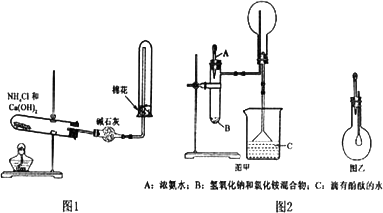
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质。某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程。提供的装置:
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是: (填装置序号)。
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
分析表中数据,实验室制NH3产率最高的是 (填序号),其它组合NH3产率不高的原因是 。
步骤二、模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式: 。
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是: 。
③D装置中的液体可换成 (填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是: 。
 2CO2+N2
2CO2+N2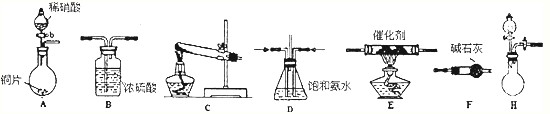
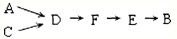

 ②氨气可使湿润的红色的石蕊试纸变蓝的原因(用方程式表示)
②氨气可使湿润的红色的石蕊试纸变蓝的原因(用方程式表示)