题目内容
【题目】下列有关叙述正确的是
A. NH3可用作制冷剂 B. 过氧化氢有氧化性,不能用于人体消毒
C. S的氧化性比Cl2的氧化性强 D. 电解饱和食盐水制备金属钠
【答案】A
【解析】A、NH3易液化,液氨气化时能带走大量的热,所以液氨可用作制冷剂,故A正确;B、过氧化氢有强氧化性,可作为人体外伤创口的消毒液,故B错误;C、S元素的非金属性比Cl元素弱,则S单质的氧化性比Cl2弱,故C错误;D、电解饱和食盐水所得产物为H2、Cl2、NaOH,工业上制备金属Na应电解熔融的NaCl,故D错误。故选A。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】氯气用于自来水的杀菌消毒,但在消毒时会产生一些负面影响,因此人们开始研究一些新型自来水消毒剂。某学习小组查阅资料发现NCl3可作为杀菌消毒剂,该小组利用下图所示的装置制备NCl3,并探究NCl3的漂白性。
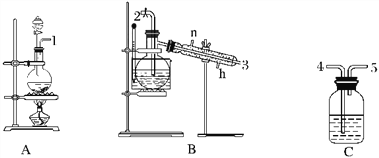
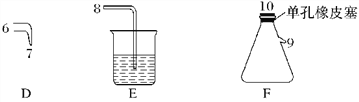
NCl3的相关性质如下:
物理性质 | 制备原理 | 化学性质 |
黄色油状液体,熔点为-40 ℃,沸点为71 ℃,不溶于冷水,易溶于有机溶剂,密度为1.65 g·mL-1 | Cl2与NH4Cl水溶液在低温下反应 | 95 ℃爆炸,热水中能与水反应 |
回答下列问题:
(1)根据实验目的,接口连接的顺序为1→____________________________________。
(2)C装置作用是_________________________________________________________________。
(3)B装置中发生反应的化学方程式为____________________________________,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为________________。
(4)当F装置的锥形瓶内有较多黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,试纸不褪色;若取该液体滴入50~60 ℃热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,试纸先变蓝后褪色,写出有关化学反应方程式并解释实验现象:___________________________________________。