题目内容
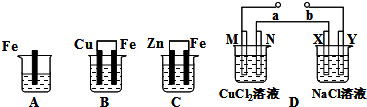
A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸
(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A ;B ;C 。
(2)一段时间后,B中Sn极附近溶液的pH (填“增大”、“减小”、“不变”)。
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度= mol·L-1。此时,三个烧杯中液体质量由大到小的顺序为: (填写序号) 。
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是 (填写序号)。
(1)A Fe+2H+=Fe2++H2↑。B Fe-2e- === Fe2+ C 2H++2e- === H2↑
(2)pH增大
(3)c(H2SO4)= 0.75 mol·L-1。 C> A=B
(4)由快到慢的顺序是 BAC
解析:略

练习册系列答案
相关题目