题目内容
【题目】Ⅰ.含氮化合物在工农业生产中都有重要应用。
(1)氨和肼(N2H4)是两种最常见的氮氢化物。
己知:4NH3(g)+3O2(g)2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g)N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为___________,该反应的化学平衡常数K=__________(用K1、K2表示)。
(2)对于2NO(g)+2CO(g)N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是____________(填字母代号)。
A.c(CO)=c(CO2) B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆 D.容器中混合气体的平均摩尔质量不变
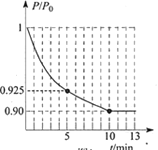
②图为容器内的压强(P)与起始压强(P0)的比值(P/P0)随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)= _____________,平衡时NO的转化率为______________。(已知气体的压强比等于其物质的量之比)
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式________________。
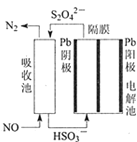
Ⅱ.采用氨水吸收烟气中的 SO2
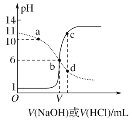
若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈_________性(填“酸”或“碱”)。 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5molLˉ1;H2SO3 : Ka1=1.3×10-2molLˉ1,Ka2=6.3×10-8molLˉ1
【答案】4NH3(g)+O2(g) 2N2H4(g)+2H2O(g) △H=+526.2kJ/mol ![]() D 0.006mol/(Lmin) 80% 2HSO3-+2e-+2H+=S2O42-+2H2O 碱
D 0.006mol/(Lmin) 80% 2HSO3-+2e-+2H+=S2O42-+2H2O 碱
【解析】
I.(1)根据盖斯定律分析解答;(2)①根据平衡状态的标志和特征结合方程式分析判断;②根据三段式,结合气体的压强比等于其物质的量之比计算解答;(3)结合图象,找出阴极的反应物、生成物,联系电极反应式书写;
Ⅱ.先计算铵根离子与亚硫酸根的水解平衡常数,再进行判断。
I.(1)①4NH3(g)+3O2(g)2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,②N2H4(g)+O2(g)N2(g)+2H2O(g) ΔH2=-534kJ/mol,根据盖斯定律,反应①-反应②×2即可消去N2,从而得到NH3和O2制取N2H4(g)的热化学方程式:4NH3(g)+O2(g) 2N2H4(g)+2H2O(g)△H =△H1-△H2×2 =-541.8kJ/mol+534kJ/mol×2 =526.2kJ/mol,则K=![]() ,故答案为:4NH3(g)+O2(g) 2N2H4(g)+2H2O(g) △H=+526.2kJ/mol;
,故答案为:4NH3(g)+O2(g) 2N2H4(g)+2H2O(g) △H=+526.2kJ/mol;![]() ;
;
(2)①对于2NO(g)+2CO(g)N2(g)+2CO2(g),①A、c(CO)=c(CO2),浓度相等不表示浓度不变,不能说明达到平衡状态,故A错误;B、由于该反应气体的质量不变,体积不变,则密度为定值,所以容器中混合气体的密度不变,不能说明是平衡状态,故B错误;C、v(N2)正=2v(NO)逆,速率不与计量系数成正比,不能说明是平衡状态,故C错误;D、由于气体的质量不变,但气体物质的量反应前后在变化,则混合气体的平均摩尔质量为变量,因此容器中混合气体的平均摩尔质量不变可以说明达到平衡状态,故D正确;故答案为:D;
②由题知起始量0.1mol NO和0.3mol CO,设N2变化量为xmol,

根据气体的压强比等于其物质的量之比,则5min时![]() =
=![]() =
=![]() ,解得x=0.03mol,v(N2)=
,解得x=0.03mol,v(N2)=![]() =
=![]() =
=![]() = 0.006mol/(Lmin);平衡时,
= 0.006mol/(Lmin);平衡时,![]() =
=![]() ,解得x=0.04mol,平衡时NO的转化率α(NO)=
,解得x=0.04mol,平衡时NO的转化率α(NO)=![]() ×100%=80%,故答案为:0.006mol/(Lmin);80%;
×100%=80%,故答案为:0.006mol/(Lmin);80%;
(3)由图可知阴极为HSO3-放电生成S2O42-,结合电子转移、电荷守恒得出电极反应式为:2HSO3-+2e-+2H+=S2O42-+2H2O,故答案为:2HSO3-+2e-+2H+=S2O42-+2H2O;
Ⅱ.①Kh(NH4+)=![]() =
=![]() ≈5.6×10-10,Kh(SO32-)=
≈5.6×10-10,Kh(SO32-)=![]() =
=![]() ≈1.6×10-7,由于Kh(NH4+)<Kh(SO32-),即铵根离子水解程度小于亚硫酸根离子的水解程度,因此亚硫酸铵溶液呈碱性,故答案为:碱。
≈1.6×10-7,由于Kh(NH4+)<Kh(SO32-),即铵根离子水解程度小于亚硫酸根离子的水解程度,因此亚硫酸铵溶液呈碱性,故答案为:碱。

【题目】如下图所示,下列关于实验现象的描述正确的是( )
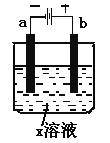
a电极 | b电极 | x溶液 | 实验现象 | |
A | 石墨 | 石墨 | CuCl2 | a电极质量增加,b电极放出无色气体 |
B | Fe | 石墨 | KNO3 | a电极质量增加,b电极放出无色气体 |
C | Fe | Cu | CuSO4 | a电极质量增加,b电极质量减少 |
D | 石墨 | 石墨 | HCl | A电极放出无色气体,b电极放出无色气体 |
A.AB.BC.CD.D
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D