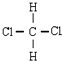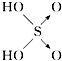题目内容
【题目】有一个未完成的离子方程式:[]+XO3﹣+6H+=3X2+3H2O,据此判断下列说法正确的是( )
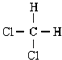
A.X2的电子式为 ![]()
B.X元素在周期表中处于ⅤA族
C.X元素的原子最外电子层上有7个电子
D.X可能是周期表中第二周期元素
【答案】C
【解析】解:根据离子方程式左右电荷相等,则未知物应含有5个负电荷,
根据方程式遵循质量守恒定律可知,如生成3molX2 , 则XO3﹣为1mol,未知物为5mol,
所以1mol未知物含有1mol负电荷,即X的最低化合价为﹣1价,
最X原子核外有7个电子,最高化合价为+7价.
A.X的最外层有7个电子,X﹣X之间有1对共用电子对,故A错误;
B.X原子核外有7个电子,应位于周期表第ⅦA族,故B错误;
C.由以上分析可知,X元素的原子最外电子层上有7个电子,故C正确;
D.X可为Cl、Br、I等元素,不为第二周期元素,故D错误.
故选:C.

练习册系列答案
相关题目
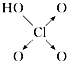
【题目】判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.含氧酸酸性强弱与非羟基氧原子数的关系如表所示:
含氧酸 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
结构式 | Cl﹣OH |
|
|
|
非羟基氧原子数 | 0 | 1 | 2 | 3 |
酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
已知:亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出:
①H3PO3的结构式为 , H3PO3与过量的NaOH溶液反应的化学方程式为;
②H3AsO3的结构式为 , 在H3AsO3中加入浓盐酸,反应的化学方程式为 .