题目内容
已知2SO2(g)+O2(g)?2SO3(g)△H=-a kJ?mol-1(a>0).恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放热0.025a kJ.下列判断正确的是( )
分析:A.根据反应热计算参加反应的二氧化硫的物质的量,再根据v=
计算v (SO2);
B.平衡后再充入0.1molSO3,平衡向逆反应移动,但移动的结果不会消除SO3含量增大;
C.根据硫元素守恒进行解答;
D.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,所到达的平衡,相当于在在原平衡基础上增大压强,平衡向正反应移动,反应物的转化率较原平衡大.
| ||
| △t |
B.平衡后再充入0.1molSO3,平衡向逆反应移动,但移动的结果不会消除SO3含量增大;
C.根据硫元素守恒进行解答;
D.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,所到达的平衡,相当于在在原平衡基础上增大压强,平衡向正反应移动,反应物的转化率较原平衡大.
解答:解:A.2min达到平衡状态,反应放热0.025a kJ,故参加反应的二氧化硫的物质的量为:2mol×
=0.05amol,故v (SO2)=
=0.0025 mol?L-1?min-1,故A错误;
B.平衡后再充入0.1molSO3,平衡向逆反应移动,但移动的结果不会消除SO3含量增大,故重新达平衡后三氧化硫的质量分数增大,故B错误;
C.开始投入0.1molSO2,容器内S原子的物质的量为0.1mol,反应混合物中二氧化硫、三氧化硫中含有S原子,故c(SO2)+c(SO3)=0.01 mol?L-1,故C正确;
D.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,所到达的平衡,相当于在在原平衡基础上增大压强,平衡向正反应移动,反应物的转化率较原平衡大,则平衡后反应放热大于0.025a kJ,故D错误;
故选C.
| 0.025akJ |
| akJ |
| ||
| 2min |
B.平衡后再充入0.1molSO3,平衡向逆反应移动,但移动的结果不会消除SO3含量增大,故重新达平衡后三氧化硫的质量分数增大,故B错误;
C.开始投入0.1molSO2,容器内S原子的物质的量为0.1mol,反应混合物中二氧化硫、三氧化硫中含有S原子,故c(SO2)+c(SO3)=0.01 mol?L-1,故C正确;
D.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,所到达的平衡,相当于在在原平衡基础上增大压强,平衡向正反应移动,反应物的转化率较原平衡大,则平衡后反应放热大于0.025a kJ,故D错误;
故选C.
点评:本题考查化学反应速率的计算、反应热的有关计算、化学平衡的移动,难度中等,注意D选项构建平衡建立的途径进行比较.

练习册系列答案
相关题目
已知2SO2(g)+O2(g)═2SO3(g),△H=-197.8kJ?mol-1,则反应:SO3 (g)═
O2 (g)+SO2 (g)的△H是( )
| 1 |
| 2 |
| A、+197.8kJ?mol-1 |
| B、+98.9kJ?mol-1 |
| C、-296.7kJ?mol-1 |
| D、-98.9kJ?mol-1 |
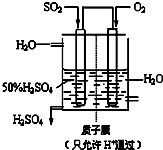
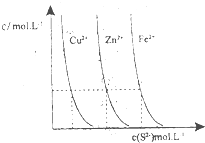 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: