题目内容
煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10?3mol·L?1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO | SO | NO | NO | Cl? |
c/(mol·L?1) | 8.35×10?4 | 6.87×10?6 | 1.5×10?4 | 1.2×10?5 | 3.4×10?3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________增加压强,NO的转化率__________(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______________(填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率__________脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反 应中,在反应ClO +2SO
+2SO ==2SO
==2SO +Cl?的平衡常数K表达式为__________。
+Cl?的平衡常数K表达式为__________。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。已知下列反应:
SO2(g)+2OH?(aq)==SO (aq)+H2O(l)ΔH1
(aq)+H2O(l)ΔH1
ClO?(aq)+SO (aq)==SO
(aq)==SO (aq)+Cl?(aq)ΔH2
(aq)+Cl?(aq)ΔH2
CaSO4(s)==Ca2+(aq)+SO (aq)ΔH3
(aq)ΔH3
则反应SO2(g)+Ca2+(aq)+ClO?(aq)+2OH?(aq)==CaSO4(s)+H2O(l)+Cl?(aq)的ΔH=____________。
某无色溶液中可能存在如下几种阴阳离子:
阳离子 | Al3+、Fe2+、Ba2+、Na+、NH4+ |
阴离子 | Cl—、CO32—、SO4 |
现对该溶液样品进行以下研究:
Ⅰ.向溶液中加入稀盐酸后有无色气体生成,该气体遇空气变成红棕色;
Ⅱ.若向Ⅰ所得溶液中加入BaCl2溶液,有白色沉淀生成;
Ⅲ.若向Ⅰ所得溶液中加入过量NaOH浓溶液并加热,产生有刺激性气味的气体,最终溶液无沉淀生成;
Ⅳ.向Ⅲ所得溶液中通入过量的CO2气体,有白色絮状沉淀生成。
根据上述实验,回答下列问题:
(1)该溶液中一定存在的阳离子为 ,一定不存在的离子为 。
(2)检验溶液中可能还存在的阳离子的方法为 。
(3)写出实验Ⅰ发生反应的离子方程式: 。
(4)写出实验Ⅳ中生成白色絮状沉淀的化学方程式: 。
下列有关实验事实的解释中正确的是
选项 | 问题 | 解释 |
A | 实验室不能配制含有Fe3+、MnO4-、SO42-、Ba2+的中性溶液 | Fe3+水解呈酸性 |
B |
| 含有Ag+的溶液必然含有NO3-,在酸性条件下,可氧化Fe2+ |
C | 将氨气通入水中,形成的水溶液能导电 | 氨气是电解质 |
D | 在FeBr2溶液中通入过量Cl2,溶液变为棕黄色 | 发生反应2Fe2++Cl2===2Fe3++2Cl- |
| A. | SO2 | B. | NO | C. | NO2 | D. | NH3 |

(1)B装置的作用是检验产物中是否有水生成.
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有SO2气体产生,写出D中发生反应的离子方程式SO2+H2O2+Ba2+=BaSO4↓+2H+.若去掉C,能否得出同样结论否(填“是”或“否”),原因是若有SO3也有白色沉淀生成.
(3)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3,而不含FeO,请帮他完成表中内容.(试剂,仪器和用品自选)
| 实验步骤 | 预期现象 | 结论 |
| 取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解;将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液 | 若高锰酸钾溶液不褪色,加入KSCN溶液后变红 | 固体残留物仅为Fe2O3 |
(5)结合上述实验现象,完成硫酸亚铁铵在500℃时隔绝空气加热完全分解的化学方程式2(NH4)2Fe(SO4)2═Fe2O3+2 NH3↑+N2↑+4SO2↑+5H2O.



 +Br2+H2O―→SO
+Br2+H2O―→SO +2Br-+2H+。某溶液中可能含有Na+、NH
+2Br-+2H+。某溶液中可能含有Na+、NH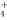 、Fe2+、K+、Br-、SO
、Fe2+、K+、Br-、SO
 2—、NO3—、I—
2—、NO3—、I— 含有H+、Fe2+的溶液中不能大量存在Ag+
含有H+、Fe2+的溶液中不能大量存在Ag+