题目内容
 慢慢加入下列物质,其中能使浓度为0.5mol?L-1的CuSO4溶液的导电能力变化如图所示的是( )
慢慢加入下列物质,其中能使浓度为0.5mol?L-1的CuSO4溶液的导电能力变化如图所示的是( )| A、蒸馏水 | B、KCl晶体 | C、NaOH溶液 | D、Ba(OH)2溶液 |
分析:溶液导电能力的强弱主要取决于阴、阳离子浓度的大小,离子浓度越大,导电能力越强,以此分析.
解答:解:A、CuSO4溶液加入蒸馏水降低了阴、阳离子的浓度,导电能力减弱,故A错误;
B、KCl晶体溶于水电离出钾离子、氯离子,增大了溶液中阴、阳离子浓度,故B错误;
C、CuSO4溶液加入NaOH溶液,铜离子与氢氧根离子反应生成氢氧化铜沉淀,消耗了铜离子同时引入钠离子,阴、阳离子数目变化不大,但溶液体积增大,阴、阳离子浓度减小,导电能力减弱,故C错误;
D、CuSO4溶液加入Ba(OH)2溶液因CuSO4与Ba(OH)2反应生成硫酸钡沉淀和氢氧化铜沉淀而使阴、阳离子浓度减小,导电能力减弱,当硫酸铜反应完全后,再加入Ba(OH)2溶液,离子浓度增大,导电能力增强,故D正确;
故选:D.
B、KCl晶体溶于水电离出钾离子、氯离子,增大了溶液中阴、阳离子浓度,故B错误;
C、CuSO4溶液加入NaOH溶液,铜离子与氢氧根离子反应生成氢氧化铜沉淀,消耗了铜离子同时引入钠离子,阴、阳离子数目变化不大,但溶液体积增大,阴、阳离子浓度减小,导电能力减弱,故C错误;
D、CuSO4溶液加入Ba(OH)2溶液因CuSO4与Ba(OH)2反应生成硫酸钡沉淀和氢氧化铜沉淀而使阴、阳离子浓度减小,导电能力减弱,当硫酸铜反应完全后,再加入Ba(OH)2溶液,离子浓度增大,导电能力增强,故D正确;
故选:D.
点评:本题考查电解质溶液的导电性,题目难度中等,注意从离子反应的角度去分析电解质溶液阴、阳离子浓度的大小,离子浓度越大,导电能力越强.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种.
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为: .
(2)实验室用二氧化锰制取氯气的化学方程式为: ;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号).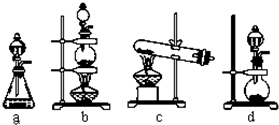
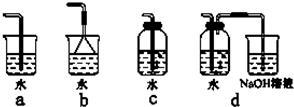
(3)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为: ;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是 (选填下列选项的编号字母).
(4)实验室制备氯气的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如下图),再把已称好50.0g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应.观察读数变化如下表所示:

请你据此分析计算:
①实验中产生的CO2气体质量为 ;
②残余液中盐酸的物质的量浓度为(结果精确到小数点后一位) .
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:
(2)实验室用二氧化锰制取氯气的化学方程式为:

(3)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为:

(4)实验室制备氯气的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如下图),再把已称好50.0g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应.观察读数变化如下表所示:

| CaCO3用量 | 未加CaCO3时 | 加约四分之一时 | 加一半时 | 全部加完时 |
| 读数/g | 318.3 | 325.3 | 334.5 | 359.5 |
①实验中产生的CO2气体质量为
②残余液中盐酸的物质的量浓度为(结果精确到小数点后一位)