题目内容
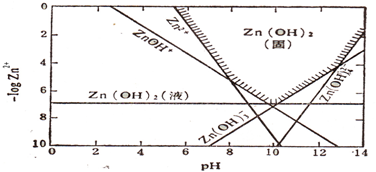
已知向Zn2+的溶液中滴加氨水,生成Zn(OH)2白色沉淀;但是氨水过量时沉淀又溶解,生成了[Zn(NH3)4]2+。此外Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液(生成ZnO现有4组离子,每组有2种金属离子。请各选用一种试剂将它们分开。可供选用的试剂有①H2SO4(aq) ②HCl(aq) ③HNO3(aq) ④NaOH(aq) ⑤氨水
请填写下表。
离子组 | 选用试剂(代号) | 沉淀化学式 | 保留在溶液中的离子 |
(1)Zn2+和Al3+ |
|
|
|
(2)Zn2+和Mg2+ |
|
|
|
(3)Zn2+和Ba2+ |
|
|
|
(4)Fe3+和Al3+ |
|
|
|
解析:离子的“检验”“分离”都是利用了离子及其化合物的化学特性来进行的。
(1)由于Zn(OH)2、Al(OH)3均为两性氢氧化物,结合题干对Zn2+性质的暗示性描述,可选“过量”氨水分离之,此时Zn2+→[Zn(NH3)4]2+,而Al3+→Al(OH)3↓。
(2)Zn2+和Mg2+的分离,可选用“过量”NaOH溶液,此时,Zn2+→ZnO![]() ,Mg2+→Mg(OH)2↓。
,Mg2+→Mg(OH)2↓。
(3)可选用H2SO4分离Zn2+和Ba2+,此时Ba2+→BaSO4↓,而Zn2+与H2SO4不反应。
(4)可利用Al(OH)3的两性特点,采取加过量NaOH溶液的方法分离Fe3+和Al3+,此时Fe3+→Fe(OH)3↓,Al3+→AlO![]() 。
。
答案:(1)⑤ Al(OH)3 [Zn(NH3)4]2+
(2)④ Mg(OH)2 ZnO![]() 或⑤ Mg(OH)2 [Zn(NH3)4]2+
或⑤ Mg(OH)2 [Zn(NH3)4]2+
(3)① BaSO4 Zn2+
(4)④ Fe(OH)3 AlO![]()

已知向Zn2+离子溶液中滴加氨水,生成白色沉淀Zn(OH)2 ;但是氨水过量时,沉淀又溶解,生成了Zn(NH3)42+。此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物。
现有4组离子,每组有2种金属离子。请各选用1种试剂将它们区分开来。可供选用的试剂有:A.硫酸,B.盐酸,C.硝酸,D.NaOH溶液,E.氨水。
请填写下表:(填写时用字母代号)
离子组 | 选用的试剂 (填字母代号) | 沉淀物的化学式 | 保留在溶液中的离子 |
⑴ Zn2+和Al3+ |
|
|
|
⑵ Zn2+和Mg2+ |
|
|
|
⑶ Zn2+和Ba2+ |
|
|
|
⑷ Fe3+和Al3+ |
|
|
|
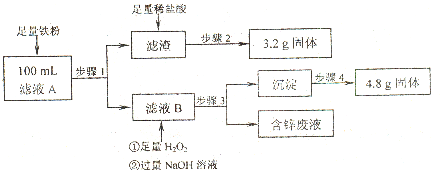

 (2011?肇庆二模)请回答有关锌及其化合物的问题.
(2011?肇庆二模)请回答有关锌及其化合物的问题. Zn2+(aq)+2OH-(aq),而Ksp[Zn(OH)2]>Ksp(ZnS),滴入的S2-与Zn2+结合生成了更难溶(或溶度积更小)的ZnS,使Zn2+浓度减小,溶解平衡继续向右移动直至全部转化为ZnS
Zn2+(aq)+2OH-(aq),而Ksp[Zn(OH)2]>Ksp(ZnS),滴入的S2-与Zn2+结合生成了更难溶(或溶度积更小)的ZnS,使Zn2+浓度减小,溶解平衡继续向右移动直至全部转化为ZnS