题目内容
19.节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若宁波全市的140余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨.甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2?CH3OH.请根据图示回答下列: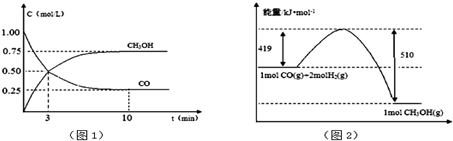
(1)关于该反应的下列说法中,正确的是C(填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,净测得CO和CH3OH(g)的浓度随时间变化如(图1)所示.从反应开始到平衡,CO的平均反应速率v(CO)=0.075mol/(L•min),该反应的平衡常数K=$\frac{4}{9}$.
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有C.
A.升高温度 B.充入He气 C.再充入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量=25.6g/mol.
(5)根据(图2),写出此反应的热化学方程式CO(g)+2H2(g)=CH3OH(g)△H=-91kJ/mol.
分析 (1)根据方程式可知,该反应为气体体积减小的反应,根据图2可知,生成物质能量低于反应;
(2)根据图I时,反应中CO浓度的变化,结合速率公式计算,根据K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$计算平衡常数;
(3)恒容条件下,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(CO)}$增大,则平衡正移,据此分析;
(4)根据平均摩尔质量=$\frac{总质量}{总物质的量}$计算;
(5)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式.
解答 解:(1)根据方程式可知,该反应为气体体积减小的反应,所以该反应△S<0,根据图2可知,生成物质能量低于反应,所以△H<0,故选C;
(2)由图I可知,反应中CO浓度的变化为:1.00-0.25=0.75mol•L-1,则v(CO)=$\frac{△c}{△t}$=$\frac{0.75mol/L}{10min}$=0.075mol/(L•min),根据图可知,平衡时c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,c(H2)=1.5mol/L,K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$=$\frac{0.7{5}^{2}}{1.{5}^{2}×0.25}$=$\frac{4}{3}$,
故答案为:0.075mol/(L•min);$\frac{4}{3}$;
(3)恒容条件下,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(CO)}$增大,则平衡正移;
A.已知该反应的正方向为放热反应,升高温度,平衡逆移,故A错误;
B.充入He气,容器的体积不变,各反应物的浓度不变,平衡不移动,故B错误;
C.再充入1molCO和2molH2,与原来加入了的量等比例,平衡时比原来的平衡的压强增大,平衡正移,故C正确;
D.使用催化剂,同等程度的改变正逆反应速率,平衡不移动,故D错误;
故答案为:C;
(4)由平衡时密度可知,平衡后混合气体的物质的量为起始时的$\frac{1}{1.6}$,平衡时总物质的量为(1mol+2mol+1mol)×$\frac{1}{1.6}$=2.5mol,总质量为1×28g+2×2g+1×32g=64g,所以平均摩尔质量=$\frac{64g}{2.5mol}$=25.6g/mol,
故答案为:25.6;
(5)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,
故答案为:CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol.
点评 本题为综合性习题,考查影响化学平衡的因素、热化学反应、化学平衡常数、反应速率的计算,图象的分析和利用等知识点,注重对高考热点知识的考查,是较好的习题,题目难度中等.

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案| A. | 纯净的二氧化硅具有良好光学性能,可用于制作光导纤维 | |
| B. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| C. | BaCO3难溶于水,可用作胃透视检查时的钡餐 | |
| D. | NaHCO3受热易分解,可用作焙制糕点的膨松剂 |
| A. | 7.69mol/L 14.5% | B. | 8.15 mol/L 15.4% | ||
| C. | 7.69 mol/L 15.4% | D. | 8.17 mol/L 14.5% |
| A. | C5H12 | B. | C3H8 | C. | C2H4Cl2 | D. | C |
| A. | X和Y能够形成能使澄清石灰水变浑浊的常见气体 | |
| B. | X、Y和Z能形成化学式为Z2XY3的化合物,该物质水溶液呈碱性 | |
| C. | X、Y、Z的原子半径:Z>X>Y | |
| D. | Y和Z只能形成一种化合物 |



 某同学在学习了乙醇的知识后,设计了如图所示的实验.操作步骤及观察到的现象如下:
某同学在学习了乙醇的知识后,设计了如图所示的实验.操作步骤及观察到的现象如下: