题目内容
肼(N2H4)—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。下列说法中,不正确的是
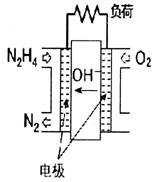
A.该电池放电时,通入肼的一极为负极
B.电池每释放1mol N2转移的电子数为4NA
C.通入空气的一极的电极反应式是:O2+2H2O+4e-=4OH-
D.电池工作一段时间后,电解质溶液的pH将不变
【答案】
D
【解析】原电池中负极失去电子,所以肼在负极通入,A正确。肼中氮元素的化合价是-2价,氧化产物是氮气,所以每释放1mol N2转移的电子数为4NA,B正确。氧气在正极通入,C正确。由于总反应式为N2H4+O2=N2+2H2O,所以氢氧化钾的浓度会降低,pH减小,D不正确。答案选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
肼(N2H4)--空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O.下列关于该电池工作时说法中正确的是( )
| A、溶液的pH保持不变 | B、溶液中的阴离子向正极移动 | C、正极的电极反应式:O2+4H++4e-=2H2O | D、负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |