题目内容
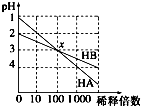 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述错误的是( )
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述错误的是( )分析:由图可知,HA开始的pH=1,稀释100倍pH=3,则HA为强酸,而HB开始的pH=2,稀释100倍pH=3,则HB为弱酸,并根据酸碱中和及电离来解答.
解答:解:A.HA开始的pH=1,稀释100倍pH=3,则HA为强酸,故A正确;
B.稀释前,c(HA)=0.1mol/L,c(HB)>0.01mol/L,则c(HA)<10c(HB),故B错误;
C.HB是弱电解质,在HB溶液中存在电离平衡,所以在x点HB未完全电离,故C正确;
D.x点,两种溶液中氢离子浓度相等,根据电荷守恒知,c(H+)=c(A-),c(H+)=c(B-),所以c(A-)=c(B-),故D正确;
故选B.
B.稀释前,c(HA)=0.1mol/L,c(HB)>0.01mol/L,则c(HA)<10c(HB),故B错误;
C.HB是弱电解质,在HB溶液中存在电离平衡,所以在x点HB未完全电离,故C正确;
D.x点,两种溶液中氢离子浓度相等,根据电荷守恒知,c(H+)=c(A-),c(H+)=c(B-),所以c(A-)=c(B-),故D正确;
故选B.
点评:本题考查电解质在水中的电离及图象,明确图象中pH的变化及交点的意义是解答本题的关键,题目难度不大.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目