题目内容
水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32—+O2+aOH-=Y+S4O62—+2H2O,下列说法中,不正确的是( )
| A.a=4 |
| B.Y的化学式为Fe2O3 |
| C.S2O32—是还原剂 |
| D.每有1 mol O2参加反应,转移电子的总物质的量为4 mol |
B
解析

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列叙述正确的是
| A.10 g H218O含有的中子数为5NA |
| B.1 mol羟基(-OH)含有的电子数为10NA |
| C.1 mol 氯气参加反应时,电子转移数目一定为2NA |
| D.标准状况下,11.2L己烷含有的分子数为0.5 NA |
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是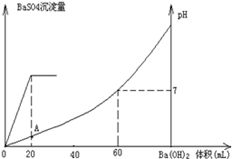
| A.图中A点溶液的pH=1 |
| B.生成沉淀的最大质量为2.33g |
| C.原混合溶液中盐酸物质的量浓度为0.1mol/L |
D.当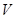 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO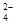 ═BaSO4↓ ═BaSO4↓ |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为9NA |
| B.pH=1的稀硫酸中含有的H+数为0.1NA |
| C.7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| D.3 mol NO2和足量H2O反应,转移NA个电子 |
下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
| A.10 g NaOH固体溶解在水中配成250 mL溶液 |
| B.将80 g SO3溶于水并配成1 L的溶液 |
| C.将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 |
| D.标准状况下,将22.4 L氯化氢气体溶于水配成1 L溶液 |
如图是氨气与氯化氢反应的装置。抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )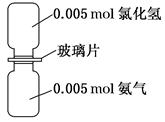
| A.气体反应物的总体积为0.224 L |
| B.生成物的分子个数为0.005NA |
| C.生成物中的N—H键个数为0.02NA |
| D.加水溶解后所得溶液中NH4+数目为0.005NA |
标准状况下,m1g气体A与m2g气体B的分子数相等,下列说法中正确的是( )
A.1个A分子的质量是1个B分子的质量的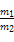 倍 倍 |
B.同温同体积的A与B的质量比为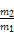 |
C.同温同质量的A与B的分子数比为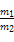 |
D.同温同压下A与B的密度比为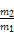 |
在(NH4)2Fe(SO4)2溶液中逐滴加入100 mL 1 mol/L的Ba(OH)2溶液,把所得沉淀过滤、洗涤、干燥,得到的固体质量不可能是( )
| A.35.3 g | B.33.5 g | C.32.3 g | D.11.3 g |