题目内容
【题目】甲醇是重要的化工原料,又可作为燃料。工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2 (g)![]() CH3OH(g) △H1;
CH3OH(g) △H1;
②CO2 (g)+3H2 (g)![]() CH3OH(g)+H2O(g) △H=-58kJ/mol;
CH3OH(g)+H2O(g) △H=-58kJ/mol;
③CO2 (g)+H2(g)![]() CO(g)+H2O(g) △H==+41k J/ mol。
CO(g)+H2O(g) △H==+41k J/ mol。
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下表:
化学键 | H—H | C-O | C≡O | H-O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=___________。
(2)合成气组成n(H2)/n(CO+ CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图甲所示。α(CO)值随温度升高而___________(填“增大”或“减小”),其原因是_____;图中的压强由大到小为___________,其判断理由是_____________。

(3)若将1mol CO2和2molH2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应②。测得CH3OH的物质的量随时间的变化如图所示。

①曲线I、Ⅱ对应的平衡常数大小关系为K1___________KⅡ(填“>”“=”或“<”)。
②一定温度下,下列能判断该反应达到化学平衡状态的是___________(填序号)。
a.容器中压强不变 b.甲醇和水蒸气的体积比保持不变
c.v正(H2)=3v逆(CH3OH) d.2个C=0断裂的同时有6个H-H断裂
③若5min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为____,该温度下的平衡常数为___________;若容器容积不变,下列措施可增加甲醇产率的是___________。(填序号)。
a.缩小反应容器的容积 b.使用合适的催化剂
c.充入He d.按原比例再充入CO2和H2
【答案】413 减小 反应①为放热反应,温度升高,平衡逆向移动 ![]() ①的正反应为气体总分子数减小的反应,温度一定时,增大压强,平衡正向移动,CO的平衡转化率增大,而反应③为气体总分子数不变的反应,产生CO的量不受压强的影响,因此增大压强时,CO的转化率提高 > ac 0.06mol/(L·min) 450 ad
①的正反应为气体总分子数减小的反应,温度一定时,增大压强,平衡正向移动,CO的平衡转化率增大,而反应③为气体总分子数不变的反应,产生CO的量不受压强的影响,因此增大压强时,CO的转化率提高 > ac 0.06mol/(L·min) 450 ad
【解析】
(1)根据盖斯定律计算△H1,再由反应热=反应物总键能-生成物总键能计算键能;
2)由图可知,压强一定时,随温度的升高,CO的转化率减小,反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小;相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高;
(3)①根据题给图象分析可知,T2先达到平衡,则T2>T1;
②依据化学平衡状态判断的标志判断;
③建立三段式,由三段式计算反应速率和平衡常数;依据反应特征判断。
(1) 根据盖斯定律:②-③=①可得①,故△H1=△H2-△H3=-58kJ.mol-1-(+41kJ.mol-1)=-99kJ.mol-1,由反应热=反应物总键能-生成物总键能可得-99kJ.mol-1=(1076kJ.mol-1+2×436kJ.mol-1)-(3×x+343+465)kJ.mol-1,解得x=413 kJ.mol-1,故答案为:413;
(2)由图可知,压强一定时,随温度的升高,CO的转化率减小,反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小;相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高,故压强P3>P2>P1,故答案为:反应①为放热反应,温度升高,平衡逆向移动;P3>P2>P1;①的正反应为气体总分子数减小的反应,温度一定时,增大压强,平衡正向移动,CO的平衡转化率增大,而反应③为气体总分子数不变的反应,产生CO的量不受压强的影响,因此增大压强时,CO的转化率提高;
(3)①根据题给图象分析可知,T2先达到平衡,则T2>T1,由温度升高,平衡逆向移动,平衡常数减小,则K1>KⅡ,故答案为:>;
②a. 反应②为气体体积减小的反应,容器中压强不变说明该反应达到化学平衡状态,故正确;
b.甲醇和水蒸气均为生成物,无论反应是否达到平衡,甲醇和水蒸气的体积比均保持不变,故错误;
c.v正(H2)=3v逆(CH3OH)说明正反应速率等于逆反应速率,说明该反应达到化学平衡状态,故正确;
d.2个C=0断裂代表正反应速率,6个H-H断裂也代表正反应速率,不能说明正反应速率等于逆反应速率,不能说明该反应达到化学平衡状态,故错误;
故选ac,故答案为:ac;
③若5min后反应达到平衡状态,H2的转化率为90%,由此建立如下三段式:
CO2 (g)+3H2 (g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起(mol/L) 0.5 1 0 0
变(mol/L) 0.3 0.9 0.3 0.3
平(mol/L) 0.2 0.1 0.3 0.3
则用CO2表示的平均反应速率为0.3 mol/L/5min=0.06mol/(L·min),反应的化学平衡常数K=c(CH3OH)c(H2O)/c(CO2)c3(H2)= 0.3 mol/L×0.3 mol/L/(0.2mol/L)×(0.1mol/L)3=450;缩小反应容器的容积,增大压强,平衡右移,甲醇产率增大;使用合适的催化剂,平衡不移动,甲醇产率不变;恒容充入He,各物质浓度不变,平衡不移动,甲醇产率不变;按原比例再充入CO2和H2,相当于增大压强增大压强,平衡右移,甲醇产率增大,故选ad,故答案为:0.06mol/(L·min);450;ad。

【题目】无机化合物可根据其组成和性质进行分类,如下所示:
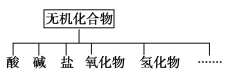
(1)上面所示的物质分类方法名称是________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥处。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②______ | ③______ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出实验室由⑩制备O2的化学方程式___________________________________。
【题目】以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)CO(g)+H2(g)△H=+131.3kJmol﹣1
①该反应在常温下_______自发进行(填“能”与“不能”);
②一定温度和压强下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是__________(填字母,下同)
a.容器中的压强不变
b.1mol H﹣H键断裂的同时断裂2mol H﹣O
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如表三组数据:
实验组 | 温度 ℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
① | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
② | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
③ | 900 | a | b | c | d | t |
①该反应为_________(填“吸”或“放”)热反应;实验②条件下平衡常数K=___________。
②实验①中从反应开始至平衡以CO2表示的平均反应速率为V(CO2)=____________(取小数点后两位)
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)CH3H(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJmol﹣1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2, 下列措施中能使c (CH3OH)增大的是_____________.

A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1mol CO2和3mol H2.




