题目内容
12.如图1是硫酸试剂瓶标签上的内容.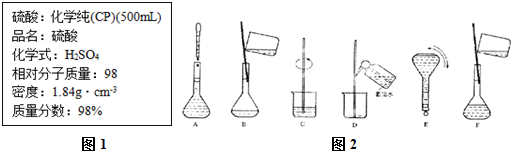
(1)该硫酸的物质的量浓度为18.4mol/L;
(2)实验室用该硫酸配制240mL0.46mol•L-1的稀硫酸,则
①需要该硫酸的体积为6.3mL;
②实验所用到的玻璃仪器除烧杯、玻璃棒外,还有量筒、250mL容量瓶和胶头滴管;
③配制过程中有几个关键的步骤和操作如图2所示:将上述实验步骤A-F按实验过程先后次序排列CBDFAE.
④该同学实际配制得到的浓度为0.45mol•L-1,可能的原因是CD
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度.
分析 (1)根据物质的量浓度c=$\frac{1000ρω}{M}$来计算;
(2)①根据溶液稀释定律C浓V浓=C稀V稀来计算;
②根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
③根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来对操作步骤来排序;
④根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)溶液的物质的量浓度c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$=18.4mol/L,故答案为:18.4mol/L;
(2)①由于实验室为240mL容量瓶,故应选用250mL容量瓶,配制出250mL溶液,设需要的浓硫酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀可知:
18.4mol/L×VmL=0.46mol/L×250mL,解得V=6.3mL,故答案为:6.3;
②根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故
除烧杯、玻璃棒外,还需要量筒、250mL容量瓶和胶头滴管.故答案为:量筒、250mL容量瓶和胶头滴管;
③根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序为CBDFAE,故答案为:CBDFAE;
④实际配制得到的浓度为0.45mol•L-1,比所要配制的浓度偏低.
A.量取浓H2SO4时仰视刻度,则浓硫酸的体积偏大,浓度偏高,故A错误;
B.容量瓶洗净后未经干燥处理,对所配溶液的浓度无影响,故B错误;
C.没有将洗涤液转入容量瓶,会导致溶质的损失,则浓度偏低,故C正确;
D.定容时仰视刻度,则溶液体积偏大,浓度偏低,故D正确.
故选CD.
点评 本题考查了一定物质的量浓度溶液的配制,注意从c=$\frac{n}{V}$理解配制原理,注意操作顺序排序中容量瓶中溶液体积多少确定BF位置.

 全能练考卷系列答案
全能练考卷系列答案| A. | 当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL | |
| B. | 当金属全部溶解时收集到NO气体的体积为4.48L(标准状况下) | |
| C. | 参加反应的金属的总质量一定是9.9g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
| A. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| B. | 标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 | |
| C. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3 NA | |
| D. | 常温下,1L 0.1 mol•L-1的Na2CO3溶液中含有的离子总数为0.3NA |
 .
.

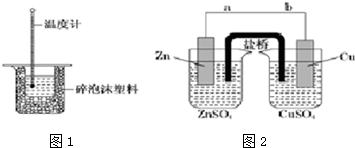
 A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.
A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.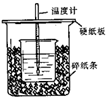 50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: